Laboratorios de Referencia
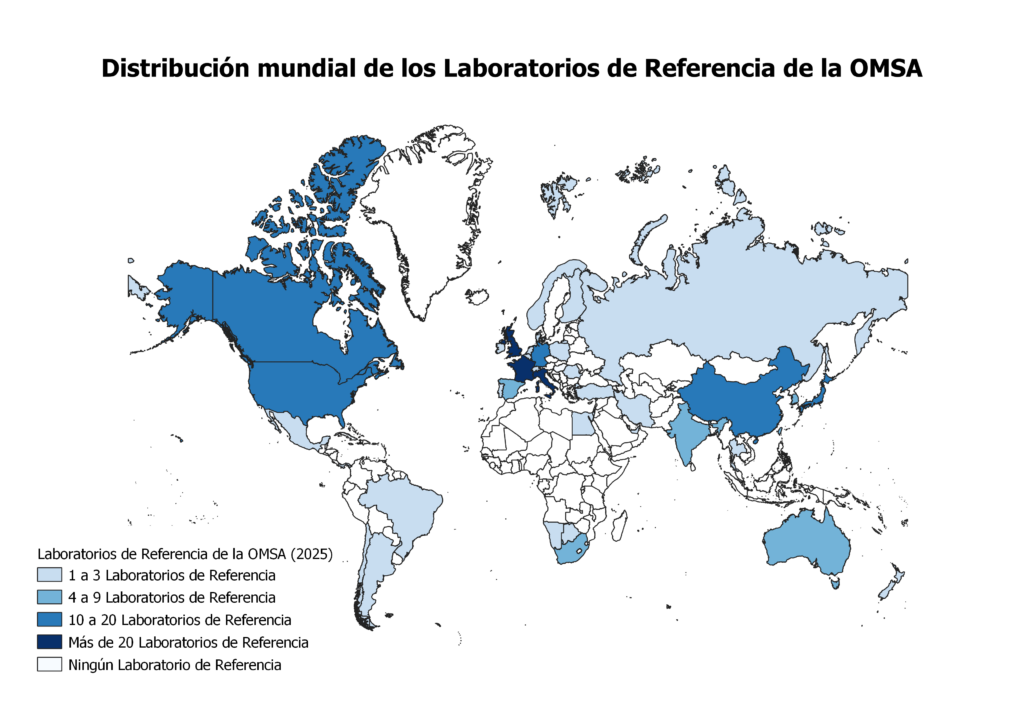
Los Laboratorios de Referencia de la OMSA son designados con el objeto de explorar todos los problemas relacionados con una enfermedad determinada. El Experto, responsable ante la OMSA y sus Países Miembros con respecto a estos asuntos, deberá ser un investigador destacado y activo en este campo para que el Laboratorio de Referencia pueda aportar asistencia científica y técnica, así como asesoramiento sobre temas relacionados con el diagnóstico y el control de la enfermedad de la que este Laboratorio de Referencia es responsable. Los Laboratorios de Referencia también deberían brindar formación científica y técnica al personal de otros Países Miembros y coordinar estudios científicos y técnicos en colaboración con otros laboratorios u organizaciones, incluyendo a través del programa de hermanamiento de la OMSA.

- Utilizar, promover y difundir los métodos de diagnóstico validados de acuerdo a los estándares de la OMSA,
- recomendar las pruebas prescritas o alternativas, o las vacunas reglas normas de la OMSA,
- desarrollar el material de referencia de acuerdo a las prescripciones de la OMSA e implementar y promover la aplicación de las normas de la OMSA,
- conservar y distribuir a los laboratorios nacionales los productos biológicos de referencia y cualquier otro reactivo utilizado para el diagnóstico y el control de los agentes patógenos o enfermedades para los cuales son designados,
- desarrollar, estandarizar y validar según las normas de la OMSA, nuevos métodos de diagnóstico y de control para el o los agentes patógenos o enfermedades para las cuales son designados,
- suministrar servicios de diagnóstico y, cuando sea apropiado, proporcionar consejos científicos y técnicos sobre las medidas de control de las enfermedades animales en los Países Miembros de la OMSA,
- liderar y/o coordinar estudios científicos y técnicos en colaboración con otros laboratorios, centros o instituciones,
- recolectar, tratar, analizar, publicar y difundir los datos epidemiológicos pertinentes sobre los agentes patógenos o las enfermedades designadas,
- comunicar informaciones científicas y técnicas a los personales de los Países Miembros de la OMSA,
- mantener un sistema de seguridad cualitativo y de de bioseguridad pertinente para los agentes patógenos y las enfermedades concernientes,
- organizar y participar en reuniones científicas en nombre de la OMSA,
- establecer y animar una red con los otros laboratorios de referencia de la OMSA designados para el mismo agente patógeno o la misma enfermedad y organizar regularmente ensayos “inter-laboratorios” para asegurar la comparabilidad de los resultados,
- organizar ensayos “inter-laboratorios” con laboratorios diferentes a los laboratorios de referencia de la OMSA para los mismos agentes patógenos o las mismas enfermedades con el fin de asegurar la equivalencia de los resultados,
- poner expertos consultores a disposición de la OMSA.
1. Ámbito e información preliminar
En mayo de 2011, la Asamblea Mundial de Delegados de la OMSA (o Asamblea) aprobó el mandato y el reglamento interno de los centros de referencia de la organización. El mandato de los laboratorios de referencia subraya la importancia de éstos para elaborar y recomendar métodos de prueba, así como para almacenar y distribuir reactivos de referencia, asesorar, prestar apoyo al diagnóstico y formación de los Países Miembros de la OMSA y ayudarles también con sus obligaciones en materia de declaración de enfermedades. A partir de 2011, el mandato incluía la recomendación de que los laboratorios establezcan y mantengan una red con los otros laboratorios de referencia de la OMSA que hayan sido designados para el mismo patógeno o la misma enfermedad, y de organizar pruebas de aptitud regularmente, entre laboratorios, para asegurarse de que los resultados son comparables, y también de organizar pruebas de aptitud con otros laboratorios, que traten sobre los mismos patógenos y enfermedades, para asegurar la equivalencia de los resultados.
Los laboratorios de referencia de la OMSA están encargados de los problemas de orden científico y técnico relacionados con una enfermedad o un agente patógeno determinados. El experto designado deberá un integrante prominente de un equipo multidisciplinario que ayude al laboratorio de referencia a proveer una asistencia científica y técnica, y un asesoramiento sobre el diagnóstico y el control de la enfermedad o el patógeno para el que es responsable el laboratorio. Los laboratorios de referencia proveerán también la formación de carácter científico y técnico para el personal de los Países Miembros, y coordinarán estudios científicos y técnicos en colaboración con otros laboratorios u organizaciones, también mediante hermanamiento con otros laboratorios.
La integridad y credibilidad de la OMSA están íntimamente relacionadas con la calidad de la ciencia a la que tiene acceso. La OMSA depende mucho de sus laboratorios de referencia, y de sus expertos, para todo lo relacionado con el asesoramiento científico y el apoyo, tanto para la sede, cuando elabora normas y la participación en los grupos ad hoc y asesoramiento en general, como para los Países Miembros.
La OMSA ha preparado el presente documento sobre el procedimiento para designar laboratorios de referencia con el fin de ayudar a los Países Miembros, a los laboratorios y a sus expertos, y a los laboratorios candidatos, a entender mejor los procedimientos que se aplican.
2. Presentación de una candidatura
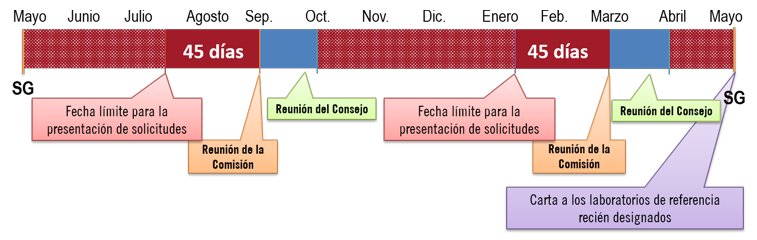
El ciclo de trabajo de la OMSA transcurre de mayo a mayo, siendo las sesiones generales de la asamblea su principio y fin. Las comisiones encargadas de examinar las candidaturas de los laboratorios se reúnen dos veces en el transcurso de cada ciclo. La primera reunión suele celebrarse a finales de agosto o principios de septiembre y la segunda entre febrero y marzo. Las fechas concretas pueden variar de año en año, en función de la disponibilidad de los miembros de las comisiones (cf. figura 1).
Se deben presentar las candidaturas 45 días antes de la fecha prevista para la reunión de la comisión pertinente. Este plazo de 45 días deja tiempo suficiente a la OMSA para examinar, traducir al inglés si procede y tramitar los expedientes para que la comisión los examine. Se deben respetar los plazos escrupulosamente, a fin de que los miembros de la comisión los puedan estudiar detenidamente antes de la reunión. Los expedientes que lleguen una vez transcurrido el plazo serán examinados en la reunión siguiente.
El laboratorio candidato presenta la información por medio del modelo que figura en las directrices para los candidatos publicadas en el sitio web de la OMSA: https://www.woah.org/es/que-ofrecemos/red-de-expertos/laboratorios-de-referencia/#ui-id-8. Los expedientes se limitarán a un máximo de 20 páginas de formato A4, a espacio simple y en Times New Roman de 10 pt. Se podrán adjuntar documentos cuya referencia figure claramente en el documento principal. Todos los documentos estarán redactados en uno de los idiomas oficiales de la OMSA (inglés, francés o español).
Al examinar el expediente, la Comisión podrá formular preguntas que se enviarán al laboratorio candidato. A tal efecto, se le enviará una carta firmada por el director general de la OMSA después de la reunión. El candidato responderá por escrito antes de que transcurra el plazo que se haya determinado, o el plazo previo a la siguiente reunión de la Comisión (45 días antes de la fecha prevista para la reunión).
3. Evaluación preliminar
Al recibir los expedientes, la sede de la OMSA (el departamento de Ciencia) acusa recibo y confirma las fechas de las reuniones de la comisión pertinente. En caso de que falte información, la sede podrá pedir que se le remita una solicitud corregida, o un suplemento de información antes de una fecha determinada.
4. Examen por la comisión especializada correspondiente
La Comisión de Normas Biológicas y la Comisión de Normas Sanitarias para los Animales Acuáticos examinan las candidaturas a laboratorio de referencia de la OMSA para las enfermedades de los animales terrestres y acuáticos respectivamente.
El mandato, el reglamento interno, la calificación y el procedimiento de elección de los miembros de las comisiones figuran en los textos fundamentales de la OMSA. Los miembros de las comisiones son elegidos o reelegidos cada tres años por la Asamblea.
Deben cumplir las obligaciones y procedimientos de confidencialidad de la OMSA, así como los relativos a los conflictos de interés. Los presidentes de las comisiones y la secretaría de la OMSA se aseguran de que los miembros para los que exista conflicto de intereses en relación a un expediente en particular no participan en las discusiones y decisiones.
De conformidad con el capítulo 3 de los criterios para designar a los centros de referencia de la OMSA y con las resoluciones que se adoptan cada año en la Sesión General para designar a los laboratorios de referencia de la OMSA para enfermedades de animales terrestres y acuáticos, todas las candidaturas son examinadas según criterios normalizados que incluyen: la capacidad, posibilidad y disposición de la institución para proveer servicios; el nivel científico y técnico de la institución en cuestión a nivel nacional e internacional; la calidad de su liderazgo científico y técnico, lo que incluye una pericia internacionalmente reconocida; las perspectivas de estabilidad de la institución en términos de personal, actividad y financiación; y la relevancia técnica y geográfica de la institución y sus actividades para las prioridades del programa de la OMSA.
Al evaluar la candidatura de un laboratorio, la comisión podrá también tomar en cuenta cualquier otra información de dominio público que se considere como pertinente para evaluar el dossier.
Conforme a los textos fundamentales de la OMSA, toda la correspondencia formal entre la comisión y organismos o personas del exterior es emitida por la oficina del director general de la OMSA. Toda la correspondencia entre un laboratorio candidato y la sede de la OMSA se documenta debidamente en la sede de la OMSA.
5. Aprobación del Consejo de la OMSA
Según el Artículo 3 del Capítulo 4 del Reglamento interno y las resoluciones pertinentes aprobadas previamente, todas las candidaturas a laboratorios de referencia de la OMSA son aprobadas por el Consejo antes de que las apruebe la Asamblea.
6. Comunicación del resultado de la evaluación al laboratorio candidato
Después de la reunión, la comisión produce un informe que contiene los resultados del examen de las candidaturas. La identidad del laboratorio candidato que la comisión recomienda aceptar se publica en el informe de la comisión. En cuanto a las candidaturas que no se aprueban, los candidatos rechazados reciben una carta del director general de la OMSA por la que se le informa del resultado del examen, con un resumen de la evaluación que incluirá, en su caso, una solicitud de clarificación o las razones del resultado negativo. Esta carta del director general de la OMSA no se publica y la identidad del laboratorio no se indica en el informe de la comisión. Algunos candidatos podrán recibir una carta con preguntas o solicitando información adicional de parte de la comisión. Esta información se enviará a la OMSA antes de que haya transcurrido el plazo fijado para que la comisión la estudie en su próxima reunión.
7. Designación de los laboratorios de referencia de la OMSA por la Asamblea
La Asamblea, en base a la evaluación de la comisión que corresponda, así como de la aprobación expresada por el Consejo de la OMSA, designará por medio de una resolución a los nuevos laboratorios de referencia de la OMSA. Las nuevas designaciones entran en vigor después de que la Asamblea haya adoptado las resoluciones.
Poco después de la Sesión General, los laboratorios de referencia recién designados recibirán una carta del director general de la OMSA. Además, la sede de la OMSA pondrá al día la lista de expertos y laboratorios en su sitio web.
8. Cambio de experto del laboratorio de referencia
Según la resolución n.º 34, adoptada por la 81.ª Sesión General en mayo de 2013, la Asamblea ha delegado al Consejo la facultad de aprobar, en su nombre, los cambios de expertos designados en los laboratorios de referencia de la OMSA, siempre y cuando los candidatos, presentados por el jefe del laboratorio de referencia por medio del delegado del país en donde esté situado el laboratorio, hayan sido examinados y ratificados por la comisión especializada pertinente.
Si el experto decide renunciar al título de experto designado y el laboratorio desea conservar la categoría de laboratorio de referencia, el delegado del país en cuestión enviará una carta oficial a la OMSA en la que detallará la situación y nombrará a un experto para el reemplazo. Adjuntará, además, el currículum vitae y la documentación del trabajo del experto en relación con la enfermedad o el patógeno. La candidatura será estudiada por la comisión pertinente en su próxima reunión y la decisión será notificada al laboratorio. El cambio oficial de experto se realizará después de la aprobación del Consejo.
Habida cuenta de las fechas de las reuniones de las comisiones y del Consejo, cabe la posibilidad de que un laboratorio de referencia se encuentre temporalmente sin experto designado. La OMSA espera que, en circunstancias normales, los laboratorios de referencia siempre cuenten con un experto designado y prevean con tiempo suficiente su jubilación o retiro. Si una comisión especializada no aprueba la nominación de un cambio de experto, el laboratorio de referencia tendrá tiempo hasta la siguiente reunión de la comisión para volver a presentar una nominación. Durante el plazo entre las reuniones, el laboratorio de referencia permanecerá en la lista de la OMSA y el nombre del experto se remplazará por la mención “Por decidir”. El laboratorio necesitará brindar un correo electrónico de trabajo que figurará en el registro de la OMSA. Si en la segunda reunión el laboratorio de referencia no presenta una nueva nominación o ésta no es validada por la comisión, se suspenderá la designación y el laboratorio de retirará de la lista de la OMSA. El laboratorio tendrá un año (dos reuniones consecutivas de las comisiones especializadas) para remplazar al experto y volver a formar parte de la lista. Transcurrido un año del retiro inicial de la lista, si no se ha validado al experto designado y la posición permanece vacante, se retirará la designación como laboratorio de referencia de conformidad con el Artículo 9 del reglamento interno (cf. Sección 10).
9. Suspensión del estatus de laboratorio de referencia de la OMSA
Se espera que los laboratorios de referencia de la OMSA cumplan su mandato y reglamento interno. Deberán contar con un experto responsable designado aprobado para la implementación de los aspectos técnicos del mandato. Si se encuentra que un laboratorio de referencia no ha podido cumplir el mandato por un cierto tiempo, por ejemplo, debido a que no se ha planificado la sucesión del experto designado lo que resulta en la ausencia de un experto designado o la falta temporal de capacidad de diagnóstico en razón de la construcción o restructuración de las instalaciones del laboratorio, el laboratorio de referencia deberá informar inmediatamente de la situación a la sede de la OMSA. La sede de la OMSA, en consulta con la comisión especializada pertinente, puede decidir la suspensión temporal de la designación del laboratorio hasta que éste pueda volver a funcionar de conformidad con las normas requeridas para los laboratorios de referencia. El periodo de suspensión no podrá ser de más de dos años. Durante este plazo, el laboratorio se retirará de la lista de la OMSA. En cualquier momento, durante estos 24 meses, se podrá restituir la designación después de que la comisión especializada haya recibido y aceptado pruebas de que el laboratorio de referencia es nuevamente operativo conforme a los requisitos exigidos. Si al cabo de los dos años, el laboratorio no puede proporcionar pruebas de su habilidad operativa, se suspenderá su designación con arreglo al Artículo 9 del reglamento interno cf. Sección 10).
10. Retiro de la designación
A partir del examen y el análisis que realiza la sede de la OMSA (cf. apartado 11.1), la comisión correspondiente estudia los informes y las actividades de los laboratorios de referencia. En caso de que no se disponga de evidencia suficiente de las actividades relativas al mandato de la OMSA, la comisión podría recomendar al Consejo y la Asamblea que se retire la designación del laboratorio.
Según el artículo 9 del capítulo 4 del reglamento interno, los laboratorios de referencia pueden ser revocados en cualquier momento. Si es el laboratorio el que decide renunciar a su designación, el delegado de su país deberá enviar una carta oficial a la OMSA.
Además, según el Artículo 9 del Capítulo 4 del reglamento interno, se le retirará la designación de laboratorio de referencia si no cumple las disposiciones del mandato y el presente reglamento. En esos casos, el director general de la OMSA, habiendo consultado a la comisión especializada apropiada y al Consejo de la OMSA, y habiendo avisado al Delegado del país, propondrá la revocación a la Asamblea.
En 2016, las comisiones y la directora general de la OMSA identificaron cinco puntos críticos a considerar cuando se evalúe el desempeño de un laboratorio, a saber:
i. ausencia de informe anual;
ii. la falta de acreditación ISO 17025 o de un sistema equivalente de gestión de la calidad, idealmente con pruebas relevantes incluidas en el ámbito de la acreditación;
iii. pauta que revela ausencia de actividad de diagnóstico o de producción y suministro de material de referencia relacionado con la enfermedad o el patógeno;
iv. no responder cuando la sede la OMSA solicite asesoramiento científico (por ejemplo, solicitud de asesoramiento técnico de Países Miembros de la OMSA, revisión de los capítulos del Manual Terrestre, etc.).
v. no haber enviado a la OMSA, cuando lo solicite, los documentos administrativos relativos a la transparencia y la confidencialidad (es decir, no renovar la declaración de conflictos de interés potenciales o no enviar el impreso sobre garantía de la confidencialidad: https://www.woah.org/es/quienes-somos/estructura/marco-de-referencia/).
11. Informe anual de los laboratorios de referencia de la OMSA
Según el artículo 8 del capítulo 4 del reglamento interno, los centros de referencia deben enviar al director general un resumen de las actividades que emanen de su mandato, al final de cada año civil y siguiendo el modelo establecido por la sede de la OMSA. El director general de la OMSA envía una carta a todos los expertos designados de los laboratorios de referencia para que presenten el informe anual.
Desde diciembre de 2013, existe la posibilidad de comunicar el informe anual en línea.
El modelo de informe anual se estructura en torno al mandato de cada laboratorio de referencia, tal como se aprobó en mayo de 2011. Las preguntas son de tipo cerrado (se responde sí o no) para obtener información más precisa y comparable. También se incluyen tablas para colectar información detallada sobre las actividades del laboratorio. Para enviar el informe anual por vía electrónica, existe una página específicaen la que se ingresa mediante un nombre de usuario y una contraseña que se envían a todos los expertos de los laboratorios de referencia por carta firmada por el director general de la OMSA el último mes del año. La fecha límite para enviar el informe suele ser finales de enero del año siguiente.
11.1. Examen y análisis de los informes anuales
Los informes recibidos son objeto de un primer examen y análisis cuantitativo, a partir de las respuestas sí o no, en la sede de la OMSA. Se presenta un resumen del análisis a la comisión correspondiente en su reunión de febrero o marzo.
Se espera de los laboratorios de referencia de la OMSA que cumplan el mandato aprobado por la Asamblea Mundial de Delegados de la OMSA que se plasma en el informe anual.
Las dudas que surjan cuando la comisión examine los informes anuales se pueden remitir al laboratorio en cuestión mediante la oficina del director general.
Todos los informes anuales de los laboratorios de referencia de la OMSA se ponen a disposición de los Países Miembros de la OMSA en su sitio web (https://www.woah.org/es/que-ofrecemos/red-de-expertos/laboratorios-de-referencia/#ui-id-5) poco después de la reunión de febrero de las comisiones.
11.2. Ausencia de informe anual
Después de las reuniones de las comisiones, se envía una carta recordatoria a los laboratorios que no han enviado todavía sus informes anuales, con copia al delegado de su país, concediendo una prórroga del plazo para enviar el informe. En cuanto a los laboratorios que a finales de marzo todavía no lo han enviado, se enviará un recordatorio directamente a su delegado, con copia al experto, fijando un plazo de dos semanas para contestar a la OMSA explicando la situación o las circunstancias que hayan podido impedir que el laboratorio cumpla esta obligación.
De ser necesario, se podrá contemplar la posibilidad de volver a entrar en comunicación, por carta o directamente durante la Sesión General, antes de formular la recomendación final de dar de baja al laboratorio en la lista, lo que haría la comisión en su reunión de septiembre. Este procedimiento se podría aplicar también a los laboratorios a los que corresponda uno de los otros cuatro criterios para el retiro de la lista (cf. Sección 10).
Contacto: [email protected]
Aborto enzoótico de las ovejas (clamidiosis ovina)
-
Dr Christiane Schnee
ALEMANIA
Address
Institute of Molecular PathogenesisFriedrich-Loeffler-InstituteFederal Research Institute for Animal Health
Naumburger Str. 96a 07743 Jena JenaContact details
+49-3641 804 2435
[email protected]
-
Dr Karine Laroucau
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Animal Health Laboratory (Maisons-Alfort), Bacterial Zoonoses Unit, 14 rue Pierre et Marie Curie, 94701 Maisons-Alfort CedexContact details
+330149771350
[email protected]
-
Dr. Nicole Borel
SUIZA
Address
Institute for Veterinary Pathology (IVPZ),
Vetsuisse Faculty, University of Zurich, Winterhurerstrasse 268, Zurich, CH-8057Contact details
+41446358571
[email protected]
Agalaxia contagiosa
-
Dr Guido Loria
ITALIA
Address
Istituto Zooprofilattico Sperimentale della Sicilia
Via G. Marinuzzi 3, 90129 PalermoContact details
+39-091 656 53 07
[email protected]
-
Dr Anne Ridley
REINO UNIDO
Address
Mycoplasma Group, Department of Statutory and Exotic Bacterial Diseases
Animal and Plant Health Agency, New Haw, Addlestone, Weybridge, Surrey KT15 3NBContact details
+44-1932 35 73 79
[email protected]
Anaplasmose
-
Dr. Juan Joel Mosqueda Gualito
MÉXICO
Address
Centro Nacional de Servicios de Constatación en Salud Animal (CENAPA)
Carretera Cuernavaca Cuautla #8534 Colonia Progreso CB 62550, Jiutepec Morelos MorelosContact details
+52-777 3.19.02.02
[email protected]
Anemia infecciosa equina
-
Dr. Maria Teresa Scicluna
ITALIA
Address
Division for the Diagnosis of Viral Diseases and Leptospirosis
Istituto Zooprofillatico Sperimentale delle Regioni Lazio e Toscana (IZSLT), Via Appia Nuova 1411, 00178 RomeContact details
+390-6 79.09.93.15
[email protected]
-
Dr Xiaojun Wang
REPÚBLICA POPULAR DE CHINA
Address
Laboratory of Equine Infectious Anemia, Harbin Veterinary Research Institute of Chinese Academy of Agricultural Sciences
427 Maduan Street, Harbin 150001Contact details
+86-189 46.06.60.85
[email protected]
Arteritis viral equina
-
To Be Decided
ESTADOS UNIDOS DE AMÉRICA
Address
Department of Veterinary Science
Maxwell H. Gluck Equine Research Center, University of Kentucky, 108 Gluck Equine Research Center Lexington, Kentucky 40546-0099Contact details
+1-859 257 47 57 ext. 81094
[email protected]
-
Prof. Falko Steinbach
REINO UNIDO
Address
Animal and Plant Health Agency
New Haw, Addlestone, Weybridge, Surrey KT15 3NBContact details
+44-1932 35 75 66
[email protected]
Babesiosis
-
Dr Valeria Blanda
ITALIA
Address
Italian Reference Centre for Anaplasma, Babesia, Rickettsia, Theileria (C.R.A.Ba.R.T.)
Istituto Zooprofilattico Sperimentale della Sicilia (IZSSi), via Gino Marinuzzi 3, 90129, PalermoContact details
+39-091 656.53.41 ext 219
[email protected]
-
Dr. Juan Joel Mosqueda Gualito
MÉXICO
Address
Centro Nacional de Servicios de Constatación en Salud Animal (CENAPA)
Carretera Cuernavaca Cuautla #8534 Colonia Progreso CB 62550, Jiutepec Morelos MorelosContact details
+52-777 3.19.02.02
[email protected]
Babesiosis bovina
-
Prof. Naoaki Yokoyama
JAPÓN
Address
Obihiro University of Agriculture and Veterinary Medicine
Obihiro University of Agriculture and Veterinary Medicine Nishi 2-13, Inada-cho Obihiro, Hokkaido 080-8555 HokkaidoContact details
+81-155 49.56.49
[email protected]
Brucelosis (Brucella abortus)
-
Dr. Heinrich Neubauer
ALEMANIA
Address
Institute of Bacterial Infections and Zoonoses, Friedrich-Loeffer Institute,
Naumburger Str. 96a, 07743 JenaContact details
+49-3641 804 2100
[email protected]
[email protected]
[email protected]
-
To be decided
ARGENTINA
Address
National Service for Agri-Food Health and Quality (SENASA)- Argentina
Talcahuano 1660, Código Postal 1640, Martinez, Buenos AiresContact details
+5491130284333
[email protected]
-
Dr. Jin-Ju Lee
COREA (REP. DE)
Address
Brucellosis Laboratory, Bacteriology DivisionAnimal and Plant Quarantine Agency (QIA)Ministry of Agriculture, Food and Rural Affairs (MAFRA)
177, Hyeoksin 8-ro, Gimcheon-si, Gyeongsangbuk-do, 39660 Gyeongsangbuk-doContact details
+82-54 912 0754
[email protected]
-
Dr Mahmoud Hamdy
EGIPTO
Address
Department of Brucellosis Research
Animal Health Research Institute, Agricultural Research Center, Ministry of Agriculture and Land Reclamation, 7 Nadi El-Said Street, P.O. Box 12618, Dokki, GizaContact details
+201 222.28.14.76
[email protected]
[email protected]
-
Prof. Ulrich Wernery
EMIRATOS ÁRABES UNIDOS
Address
Central Veterinary Research Laboratory
P.O. Box 597 Dubai DubaiContact details
+971-4 337.51.65
[email protected]
-
Dr Claire Ponsart
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Animal Health Laboratory (Maisons-Alfort), Bacterial Zoonoses Unit, 14 rue Pierre et Marie Curie, F-94701 Maisons-Alfort CedexContact details
+33149771350
[email protected]
-
Dr. Svetlana Berdenstein
ISRAEL
Address
Kimron Veterinary Institute, Department of Bacteriology
P.O. Box 12, Beit Dagan 50250Contact details
+972-3 968 16 98
[email protected]
-
Dr Fabrizio De Massis
ITALIA
Address
Istituto Zooprofilattico Sperimentaledell'Abruzzo e del Molise 'G. Caporale'
Via Campo Boario 64100 Teramo TERAMOContact details
+390-861 33 22 41
[email protected]
-
Dr Adrian Whatmore
REINO UNIDO
Address
Animal and Plant Health Agency
New Haw, Addlestone, Weybridge, Surrey KT15 3NBContact details
+44-1932 35.76.10
[email protected]
-
Prof. Liangquan Zhu
REPÚBLICA POPULAR DE CHINA
Address
WOAH/FAO/National reference laboratory for brucellosis
China Institute of Veterinary Drug Control, No. 33 Qingfeng Street, Daxing District, Beijing 102600Contact details
+861062103630
[email protected]
[email protected]
[email protected]
-
Dr. Monaya Ekgatat
TAILANDIA
Address
National Institute of Animal Health
50/2 Kasetklang Ladyao Chatuchak Bangkok 10900 THAILANDContact details
+66-2579 89.08 to 14 ext. 232
[email protected]
Brucelosis (Brucella canis)
-
Prof. Ulrich Wernery
EMIRATOS ÁRABES UNIDOS
Address
Central Veterinary Research Laboratory
P.O. Box 597 Dubai DubaiContact details
+971-4 337.51.65
[email protected]
Brucelosis (Brucella melitensis)
-
Dr. Heinrich Neubauer
ALEMANIA
Address
Institute of Bacterial Infections and Zoonoses, Friedrich-Loeffer Institute,
Naumburger Str. 96a, 07743 JenaContact details
+49-3641 804 2100
[email protected]
[email protected]
[email protected]
-
To be decided
ARGENTINA
Address
National Service for Agri-Food Health and Quality (SENASA)- Argentina
Talcahuano 1660, Código Postal 1640, Martinez, Buenos AiresContact details
+5491130284333
[email protected]
-
Dr Mahmoud Hamdy
EGIPTO
Address
Department of Brucellosis Research
Animal Health Research Institute, Agricultural Research Center, Ministry of Agriculture and Land Reclamation, 7 Nadi El-Said Street, P.O. Box 12618, Dokki, GizaContact details
+201 222.28.14.76
[email protected]
[email protected]
-
Prof. Ulrich Wernery
EMIRATOS ÁRABES UNIDOS
Address
Central Veterinary Research Laboratory
P.O. Box 597 Dubai DubaiContact details
+971-4 337.51.65
[email protected]
-
Dr Claire Ponsart
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Animal Health Laboratory (Maisons-Alfort), Bacterial Zoonoses Unit, 14 rue Pierre et Marie Curie, F-94701 Maisons-Alfort CedexContact details
+33149771350
[email protected]
-
Dr. Svetlana Berdenstein
ISRAEL
Address
Kimron Veterinary Institute, Department of Bacteriology
P.O. Box 12, Beit Dagan 50250Contact details
+972-3 968 16 98
[email protected]
-
Dr Fabrizio De Massis
ITALIA
Address
Istituto Zooprofilattico Sperimentaledell'Abruzzo e del Molise 'G. Caporale'
Via Campo Boario 64100 Teramo TERAMOContact details
+390-861 33 22 41
[email protected]
-
Dr Adrian Whatmore
REINO UNIDO
Address
Animal and Plant Health Agency
New Haw, Addlestone, Weybridge, Surrey KT15 3NBContact details
+44-1932 35.76.10
[email protected]
-
Prof. Liangquan Zhu
REPÚBLICA POPULAR DE CHINA
Address
WOAH/FAO/National reference laboratory for brucellosis
China Institute of Veterinary Drug Control, No. 33 Qingfeng Street, Daxing District, Beijing 102600Contact details
+861062103630
[email protected]
[email protected]
[email protected]
-
Dr. Monaya Ekgatat
TAILANDIA
Address
National Institute of Animal Health
50/2 Kasetklang Ladyao Chatuchak Bangkok 10900 THAILANDContact details
+66-2579 89.08 to 14 ext. 232
[email protected]
Brucelosis (Brucella suis)
-
Dr. Heinrich Neubauer
ALEMANIA
Address
Institute of Bacterial Infections and Zoonoses, Friedrich-Loeffer Institute,
Naumburger Str. 96a, 07743 JenaContact details
+49-3641 804 2100
[email protected]
[email protected]
[email protected]
-
To be decided
ARGENTINA
Address
National Service for Agri-Food Health and Quality (SENASA)- Argentina
Talcahuano 1660, Código Postal 1640, Martinez, Buenos AiresContact details
+5491130284333
[email protected]
-
Dr Claire Ponsart
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Animal Health Laboratory (Maisons-Alfort), Bacterial Zoonoses Unit, 14 rue Pierre et Marie Curie, F-94701 Maisons-Alfort CedexContact details
+33149771350
[email protected]
-
Dr Fabrizio De Massis
ITALIA
Address
Istituto Zooprofilattico Sperimentaledell'Abruzzo e del Molise 'G. Caporale'
Via Campo Boario 64100 Teramo TERAMOContact details
+390-861 33 22 41
[email protected]
-
Dr Adrian Whatmore
REINO UNIDO
Address
Animal and Plant Health Agency
New Haw, Addlestone, Weybridge, Surrey KT15 3NBContact details
+44-1932 35.76.10
[email protected]
-
Prof. Liangquan Zhu
REPÚBLICA POPULAR DE CHINA
Address
WOAH/FAO/National reference laboratory for brucellosis
China Institute of Veterinary Drug Control, No. 33 Qingfeng Street, Daxing District, Beijing 102600Contact details
+861062103630
[email protected]
[email protected]
[email protected]
Bursitis infecciosa (Enfermedad de Gumboro)
-
Dr Nicolas Eterradossi
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Ploufragan-Plouzané-Niort Laboratory, Poultry and Rabbit Virology, Immunology, Parasitology Unit, B.P. 53, 22440 PloufraganContact details
+33 (0)2 96 01 62 22
[email protected]
-
Dr. Yulong Gao
REPÚBLICA POPULAR DE CHINA
Address
Division of Avian Immunosuppressive Disease, Harbin Veterinary Research Institute (HVRI)
Chinese Academy of Agricultural Sciences (CAAS), 678 Haping Road, Xiangfang District, Harbin 150069Contact details
+8618945083045864
[email protected]
Campilobacteriosis
-
Dr. Jaap Wagenaar
PAÍSES BAJOS
Address
Department of Infectious Diseases and Immunology,
Faculty of Veterinary Medicine, trecht University, PO Box 80.165, 3508 TD UtrechtContact details
+31-320 23 81 57
[email protected]
Caquexia crónica
-
Dr. Gordon Mitchell
CANADÁ
Address
Canadian Food Inspection Agency, Ottawa Laboratory (Fallowfield), Animal Disease Research Institute
3851 Fallowfield Road, P.O. Box 11300, Station H, Nepean, Ontario K2H 8P9nContact details
+1-613 221.48.54
[email protected]
-
Dr Hyun-Joo Sohn
COREA (REP. DE)
Address
Prion Disease Research Laboratory, Division of Foreign Animal DiseaseAnimal and Plant Quarantine Agency (QIA)Ministry of Agriculture, Food and Rural Affairs (MAFRA)
177, Hyeoksin 8-ro, Gimcheon-si, Gyeongsangbuk-do, 39660 Gyeongsangbuk-doContact details
+82-54 912 0862
[email protected]
-
Dr. Aaron Lehmkuhl
ESTADOS UNIDOS DE AMÉRICA
Address
National Veterinary Services Laboratories, USDA, APHIS, VS
1920 Dayton Avenue, Ames, Iowa 50010Contact details
+15153377175
[email protected]
-
Dr. Sylvie L. Benestad
NORUEGA
Address
Norwegian Veterinary Institute (NVI)
Pb 64, N-1431 ÅsContact details
+47-23 21.60.00
[email protected]
[email protected]
Carbunco bacteridiano
-
Dr. Kingsley Amoako
CANADÁ
Address
Canadian Food Inspection Agency
National Centre for Animal Disease (NCAD), Lethbridge Laboratory, Lethbridge T1J 3Z4Contact details
+14033825505
[email protected]
Cisticercosis
-
Dr Xuenong Luo
REPÚBLICA POPULAR DE CHINA
Address
Department of Parasitology, State Key Laboratory of Veterinary Etiological Biology, Lanzhou Veterinary Research Institute,
Chinese Academy of Agricultural Sciences, 1 Xujiaping, Lanzhou, Gansu Province 730046,Contact details
+86-931 832.39.78
[email protected]
Clamidiosis aviar
-
Dr Christiane Schnee
ALEMANIA
Address
Institute of Molecular PathogenesisFriedrich-Loeffler-InstituteFederal Research Institute for Animal Health
Naumburger Str. 96a 07743 Jena JenaContact details
+49-3641 804 2435
[email protected]
-
Dr Karine Laroucau
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Animal Health Laboratory (Maisons-Alfort), Bacterial Zoonoses Unit, 14 rue Pierre et Marie Curie, 94701 Maisons-Alfort CedexContact details
+330149771350
[email protected]
Cowdriosis
-
Dr Valérie Rodrigues
FRANCIA
Address
UMR ASTRE : Animal, Santé, Territoires, Risques, Ecosystèmes ; CIRAD Département BIOS
Domaine Duclos – Prise-D'eau 97170 Petit-Bourg, GuadeloupeContact details
+33 (0)4 67 59 37 39
[email protected]
Dermatosis nodular contagiosa
-
Dr. Nick De Regge
BÉLGICA
Address
Department of Infectious Diseases in Animals
Exotic and vector-borne diseases (EXOVEC), Sciensano, Groeselenberg 99, 1180 UccleContact details
+3223790514
[email protected]
-
Georgina Limon-Vega
REINO UNIDO
Address
Pirbright,
Ash Road, Woking, Surrey GU24 0NFContact details
+44-1483 23.24.41
[email protected]
-
Dr. Antoinette Van Schalkwyk
SUDÁFRICA
Address
Senior Researcher
Onderstepoort Veterinary Institute, Agricultural Research Council, Private Bag X05, Onderstepoort 0110,Contact details
+27125299108
[email protected]
Diarrea viral bovina
-
Dr. Kerstin Wernike
ALEMANIA
Address
Institute of Diagnostic Virology
Friedrich-Loeffler-Institut Federal Research Institute for Animal Health Südufer 10 17493 Greifswald – Insel Riems Insel RiemsContact details
+49-38351 7-1212
[email protected]
-
Dr. Peter Kirkland
AUSTRALIA
Address
Elizabeth Macarthur Agriculture Institute (EMAI), Virology Laboratory
Woodbridge Rd, Menangle, PMB 8, Camden NSW 2570Contact details
+61-2 46.40.63.31
[email protected]
[email protected]
-
Dr. Oliver Lung
CANADÁ
Address
Canadian Food Inspection Agency,
National Centre for Animal Disease (NCAD), P.O. Box 640, Township Road 9-1, Lethbridge, Alberta T1J 3Z4Contact details
+1-403 382 55 00
[email protected]
-
Dr. Rebecca Strong
REINO UNIDO
Address
Animal and Plant Health Agency
New Haw, Addlestone, Weybridge, Surrey KT15 3NBContact details
+44-208 415 2102
[email protected]
Durina
-
Dr Laurent Hébert
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Animal Health Laboratory (Normandy site), Physiopathology and Epidemiology of Equine Diseases Unit, 14430 DozuléContact details
+33-(0)2 31.79.22.76
[email protected]
Encefalitis japonesa
-
Dr. Dong-Kun Yang
COREA (REP. DE)
Address
Animal and Plant Quarantine Agency
177 Hyeoksin 8-ro Gimcheong-si Gyeongsangbuk-do 39660 GyeongsangbukContact details
+82 31 467.1783
[email protected]
Encefalopatía espongiforme bovina
-
Dr. Waqas Tahir
CANADÁ
Address
Lethbridge Laboratory
Canadian Food Inspection Agency, National Centre for Animal Disease (NCAD), Lethbridge Laboratory, Lethbridge T1J 3Z4Contact details
+1-403 382.55.49
[email protected]
-
Dr Juan José Badiola Díez
ESPAÑA
Address
Centro de investigación en Encefalopatías y enfermedades transmisibles emergentes
Universidad de Zaragoza, Facultad de Veterinaria, Departamento de Patología Animal, Miguel Servet 177, 50013 ZaragozaContact details
+34-976 76 20 19
[email protected]
-
Dr. Cristina Casalone
ITALIA
Address
Italian National Reference Centre for Diagnostic Activities in Stranded Marine Mammals (C.Re.Di.Ma.), via Bologna 148, 10154 TorinoContact details
+39-11 26 86 296
[email protected]
[email protected]
-
Dr. Yoshifumi Iwamaru
JAPÓN
Address
National Agricultural Research Organization, Prion Diseases Research Unit, National Institute of Animal Health
3-1-5 Kannondai, Tsukuba, Ibaraki 305-0856Contact details
+81-29 838 83 33
[email protected]
-
Dr. John Spiropoulos
REINO UNIDO
Address
Animal and Plant Health Agency
New Haw, Addlestone, Weybridge, Surrey KT15 3NBContact details
+44 1932 357.564
[email protected]
-
Prof. Torsten Seuberlich
SUIZA
Address
Neuro Centre Department of Clinical Research and Veterinary Public Health
Division of Experimental Clinical Research, University of Bern, Bremgartenstrasse 109 A3012 Bern,Contact details
+41-31 631 22 06
[email protected]
Encefalopatía y retinopatía virales
-
Dr Anna Toffan
ITALIA
Address
Istituto Zooprofilattico Sperimentale delle Venezie, Fish Virology Dept
Viale dell'Università, 10,35020 Legnaro (Padova)Contact details
+39-049 808 43 88
[email protected]
Enfermedad de Aujeszky
-
Dre. Céline Deblanc
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Ploufragan-Plouzané-Niort Laboratory, Porcine Virology Immunology Unit, B.P. 53, 22440 PloufraganContact details
+330296016205
[email protected]
Enfermedad de Marek
-
Dr. Yongxiu Yao
REINO UNIDO
Address
The Pirbright Institute
Ash Road, Pirbright, Woking, Surrey GU24 0NFContact details
+441487231415
[email protected]
Enfermedad de Newcastle
-
Dr Christian Grund
ALEMANIA
Address
Institute of Diagnostic Virology, Friedrich-Loeffler-Institute
Federal Research Institute for Animal Health, Südufer 10, D-17493 Greifswald, Insel RiemsContact details
+49-38351 7 1196
[email protected]
-
Dra. Dilmara Reischak
BRASIL
Address
Auditora Fiscal Federal Agropecuária
Laboratório de Diagnóstico Animal, Laboratório Federal de Defesa Agropecuária – LFDA/SP – CGAL, Ministério da Agricultura, Pecuária e Abastecimento, Rua Raul Ferrari, s/n°Jardim Santa Marcelina, CEP 13100-105, Campinas SP, Sao PauloContact details
+551932522117
[email protected]
[email protected]
-
Dr Ji-Ye Kim
COREA (REP. DE)
Address
Newcastle disease Laboratory, Avian Disease division, Animal and Plant Quarantine Agency (QIA)
Ministry of Agriculture, Food and Rural Affairs (MAFRA), 177, Hyeoksin 8-ro, Gimcheon-si, Gyeongsangbuk-do, 39660Contact details
+82-54 912 0968
[email protected]
-
Dr. Mia Kim Torchetti
ESTADOS UNIDOS DE AMÉRICA
Address
National Veterinary Services Laboratories, USDA, APHIS, VS
1920 Dayton Avenue, Ames, Iowa 50010Contact details
+15153377551
[email protected]
-
Dr Isabella Monne
ITALIA
Address
Istituto Zooprofilattico Sperimentale delle Venezie, Research and Innovation Dept.
Viale Dell'Università 10, 35020 Legnaro PDContact details
+39-049 808 4381
[email protected]
-
Dr. Ashley Banyard
REINO UNIDO
Address
WOAH/FAO International Reference Laboratory for Avian Influenza
Animal and Plant Health Agency – Weybridge, Addlestone, Surrey KT15 3NBContact details
+441483232441
[email protected]
-
Dr. Hualei Liu
REPÚBLICA POPULAR DE CHINA
Address
Avian Disease Surveillance Laboratory, National Reference Laboratory for Newcastle Disease
National Surveillance and Research Center for Exotic Animal Diseases, China Animal Health and Epidemiology Center (CAHEC)Contact details
+8653285623396
[email protected]
[email protected]
-
Dr. Viktor N. Irza
RUSIA
Address
National Reference Laboratory for Avian Influenza and Newcastle Disease
Federal State-Financed Institution “Federal Centre for Animal Health” (FGBI “ARRIAH”), Yur'evets, Vladimir 60090Contact details
+7-4922 26 18 67
[email protected]
[email protected]
Enfermedad de la necrosis hepatopancreática aguda
-
Dr Arun Dhar
ESTADOS UNIDOS DE AMÉRICA
Address
Aquaculture Pathology Laboratory, School of Animal and Comparative Biomedical Sciences
University of Arizona, 1117 E Lowell St, Building 90, 85721 TucsonContact details
+1-520 621 87.27
[email protected]
-
Prof. Han-Ching Wang
TAIPEI CHINO
Address
International Center for the Scientific Development of Shrimp Aquaculture (ICDSA), National Cheng Kung University (NCKU)
No. 500, Sec. 3, Anming Road, Annan District, Tainan City 709Contact details
+886-6 384 24 48
[email protected]
Enfermedad epizoótica hemorrágica
-
Dr Stephan Zientara
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Animal Health Laboratory (Maisons-Alfort), Virology unit, 14 rue Pierre et Marie Curie, 94701 Maisons-AlfortContact details
+33149771350
[email protected]
Enfermedad hemorrágica del conejo
-
Dr. Patrizia Cavadini
ITALIA
Address
Istituto Zooprofilattico Sperimentale della Lombardia e dell'Emilia Romagna 'B. Ubertini'
Via A. Bianchi No. 7/9, 25124 Brescia,Contact details
+39-30 229 06 17
[email protected]
Enfermedad vesicular porcina
-
Giulia Pezzoni
ITALIA
Address
Istituto Zooprofilattico Sperimentale della Lombardia e dell'Emilia Romagna (IZSLER)
Via A. Bianchi No. 9, 25124 BresciaContact details
+390302290310
[email protected]
-
Dr. Donald King
REINO UNIDO
Address
The Pirbright Institute, Vesicular Disease Reference Laboratories
Ash Road, Pirbright, Woking, Surrey GU24 0NF,Contact details
+441483231021
[email protected]
Enfermedades causadas por los virus Hendra y Nipah
-
Dr. Kim Halpin
AUSTRALIA
Address
CSIRO Australian Centre for Disease Preparedness
5 Portarlington Road, Private Bag 24 (Ryrie Street), Geelong 3220, VictoriaContact details
+61-3 52 27 00 00
[email protected]
[email protected]
Epididimitis ovina (Brucella ovis)
-
To be decided
ARGENTINA
Address
National Service for Agri-Food Health and Quality (SENASA)- Argentina
Talcahuano 1660, Código Postal 1640, Martinez, Buenos AiresContact details
+5491130284333
[email protected]
-
Dr Claire Ponsart
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Animal Health Laboratory (Maisons-Alfort), Bacterial Zoonoses Unit, 14 rue Pierre et Marie Curie, F-94701 Maisons-Alfort CedexContact details
+33149771350
[email protected]
-
Dr Fabrizio De Massis
ITALIA
Address
Istituto Zooprofilattico Sperimentaledell'Abruzzo e del Molise 'G. Caporale'
Via Campo Boario 64100 Teramo TERAMOContact details
+390-861 33 22 41
[email protected]
-
Dr Adrian Whatmore
REINO UNIDO
Address
Animal and Plant Health Agency
New Haw, Addlestone, Weybridge, Surrey KT15 3NBContact details
+44-1932 35.76.10
[email protected]
Equinococosis (Echinococcus granulosus y E. multilocularis)
-
Dr Giovanna Masala
ITALIA
Address
National Reference Laboratory for Cyctic Echinococcosis (CE)
Istituto Zooprofilattico Sperimentale (IZS) of SardiniVia Duca degli Abruzzi, 807100 Sassari,, SassariContact details
+39-079 289 200
[email protected]
[email protected]
Escherichia coli
-
Dr. John Morris Fairbrother
CANADÁ
Address
The Escherichia coli Laboratory (EcL)Faculty of Veternary Medicine, University of Montreal
3200 Sicotte Saint-Hyacinthe Québec J2S 2M2 QuébecContact details
+1-450 773.85.21
[email protected]
Estomatitis vesicular
-
Dr. Edviges Maristela Pituco
BRASIL
Address
PANAFTOSA
Av. President Kennedy 7778 25040-000 Duque de Caxias Rio de Janeiro Rio de JaneiroContact details
+55-21 36.61.90.64
[email protected]
-
Dr. Rachel Tell
ESTADOS UNIDOS DE AMÉRICA
Address
National Veterinary Services Laboratories, USDA, APHIS, VS
1920 Dayton Avenue, Ames, Iowa 50010Contact details
+15153377551
[email protected]
Estreptococosis porcina
-
Prof. Chengping Lu
REPÚBLICA POPULAR DE CHINA
Address
Nanjing Agricultural University (NAU)
Branch of Swine Streptococcosis Diagnostic Laboratory (BSSDL), Weigang No.1, Nanjing, Jiangsu ProvinceContact details
+86-25 84.39.53.28
[email protected]
[email protected]
Fiebre Q
-
Dr Elodie Rousset
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Sophia-Antipolis Laboratory, Animal Q fever, 105, route des Chappes, BP 111, 06902 Sophia-AntipolisContact details
+33-4 92.94.37.00
[email protected]
-
Dr. Agnieszka Jodelko
POLONIA
Address
National Veterinary Research Institute, Department of Cattle and Sheep Diseases
Al. Partyzantow str. 5724-100 PulawyContact details
+48818893274
[email protected]
[email protected]
Fiebre aftosa
-
Dra. Sabrina Galdo
ARGENTINA
Address
Laboratorio de Fiebre Aftosa de la Dirección de Laboratorios y Control Técnico
Av. Sir. Alexander Fleming 1653 , Martínez (1640), Buenos AiresContact details
+54-11 48.36.19.95
[email protected]
[email protected]
-
Dr. Joseph Hyera
BOTSUANA
Address
Botswana Vaccine Institute
Broadhurst Industrial Site, Lejara Road, Private Bag 0031, GaboroneContact details
+2673912711
[email protected]
-
Dr. Edviges Maristela Pituco
BRASIL
Address
PANAFTOSA
Av. President Kennedy 7778 25040-000 Duque de Caxias Rio de Janeiro Rio de JaneiroContact details
+55-21 36.61.90.64
[email protected]
-
Dr. Charles Nfon
CANADÁ
Address
National Centre for Foreign Animal Disease, Canadian Food Inspection Agency
Canadian Science Centre for Human and Animal Health, 1015 Arlington Street, Suite T2300, Winnipeg, Manitoba R3E 3M4Contact details
+1-204 789.20.23
[email protected]
-
To Be Decided
COREA (REP. DE)
Address
Division of Foot and Mouth Disease, Animal and Plant Quarantine Agency (QIA), Ministry of Agriculture, Food and Rural Affairs
177, Hyeoksin 8-ro, Gimcheon-si, Gyeongsangbuk-do, 39660Contact details
+82549120774
[email protected]
-
Vivian O'Donnell
ESTADOS UNIDOS DE AMÉRICA
Address
National Veterinary Services Laboratories, USDA, APHIS, VS
40550 Route 25, Orient, New York, NY 11957Contact details
+16313233300
[email protected]
-
Dr Bakkali Kassimi Labib
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Animal Health Laboratory (Maisons-Alfort), Virology unit, 14 rue Pierre et Marie Curie, 94701 Maisons-Alfort CedexContact details
+330149771350
[email protected]
-
Santina Grazioli
ITALIA
Address
Istituto Zooprofilattico Sperimentale della Lombardia e dell'Emilia Romagna (IZSLER)
Via A. Bianchi No. 9, 25124 BresciaContact details
+390-30 229 03 10
[email protected]
-
Dr. Donald King
REINO UNIDO
Address
The Pirbright Institute, Vesicular Disease Reference Laboratories
Ash Road, Pirbright, Woking, Surrey GU24 0NF,Contact details
+441483231021
[email protected]
-
Dr Xiangtao Liu
REPÚBLICA POPULAR DE CHINA
Address
Lanzhou Veterinary Research Institute, CAAS, National Foot and Mouth Disease Reference Laboratory
Xujiaping No.1, Yanchangpu, Lanzhou, Gansu Province 730046Contact details
+86-931 834.25.85
[email protected]
[email protected]
-
Dr. Valery Zakharov
RUSIA
Address
Federal Governmental Institute, Centre for Animal Health (FGI-ARRIAH)
600900 Yur'evets, VladmirContact details
+7-4922 26 06 14
[email protected]
[email protected]
-
Dr Livio Heath
SUDÁFRICA
Address
Onderstepoort Veterinary Institute,
Agricultural Research Council, Private Bag X05, Onderstepoort 0110Contact details
+27-12 529 95.01
[email protected]
Fiebre del Nilo Occidental
-
Dr Federica Monaco
ITALIA
Address
Istituto Zooprofilattico Sperimentale dell'Abruzzo e del Molise "G. Caporale"
Via Campo Boario, 64100 TeramoContact details
+39 0861 33.22.05
[email protected]
Fiebre del Valle del Rift
-
Dre. Catherine Cetre-Sossah
FRANCIA
Address
CIRAD
Campus international de Baillarguet, TA A15/E, 34398 Montpellier Cedex 5Contact details
+33467593834
[email protected]
-
Dr Baratang Alison Lubisi
SUDÁFRICA
Address
Senior Research Veterinarian
Onderstepoort Veterinary Institute, Agricultural Research Council, Private Bag X05, Onderstepoort 0110Contact details
+27-12 529 91 17
[email protected]
Gripe equina
-
To be Decided
ESTADOS UNIDOS DE AMÉRICA
Address
Department of Veterinary Science
Maxwell H. Gluck Equine Research Center, University of Kentucky, 108 Gluck Equine Research Center, Lexington, Kentucky 40546-0099Contact details
+1-859 257 47 57
[email protected]
-
Prof. Ann Cullinane
IRLANDA
Address
Irish Equine Centre
Johnstown, Naas, Co. KildareContact details
+353-45 86.62.66
[email protected]
-
Dr Manabu Nemoto
JAPÓN
Address
Equine Research Institute, Japan Racing Association
1400-4 Shiba, Shimotsuke, Tochigi 329-0412Contact details
+81-285 44.0090
[email protected]
[email protected]
Gripe porcina
-
Dr. Mia Kim Torchetti
ESTADOS UNIDOS DE AMÉRICA
Address
National Veterinary Services Laboratories, USDA, APHIS, VS
1920 Dayton Avenue, Ames, Iowa 50010Contact details
+15153377551
[email protected]
-
Dr. Chiara Chiapponi
ITALIA
Address
Istituto Zooprofilattico Sperimentale della Lombardia e dell'Emilia Romagna
Via Bianchi 9 25124 Brescia BresciaContact details
+39 (0)52129.37.33
[email protected]
-
Dr. Junki Mine
JAPÓN
Address
Viral Disease and Epidemiology Research Division, National Institute of Animal Health, National Agriculture and Food Research Organization
Kannondai, Tsukuba, Ibaraki, 305-0856Contact details
+81298387704
[email protected]
-
Dr. Helen Everett
REINO UNIDO
Address
Virology Dept
Animal and Plant Health Agency – Weybridge, Addlestone, Surrey KT15 3NBContact details
+441483232441
[email protected]
Herpesvirosis del abalón
-
Dr. Nick Moody
AUSTRALIA
Address
CSIRO Australian Centre for Disease Preparedness
5 Portarlington Road, Private Bag 24 (Ryrie Street), Geelong 3220, VictoriaContact details
+61-3 52 27 00 00
[email protected]
Herpesvirosis del salmón masou
-
Dr. Hisae Kasai
JAPÓN
Address
Laboratory of Biotechnology and MicrobiologyFaculty of Fisheries ScienceHokkaido University
3-1-1 Minato-Cho Hakodate Hokkaido 041-8611 HOKKAIDOContact details
+81-138 40 88 98
[email protected]
Infecció por el virus del síndrome de Taura
-
Dr Arun Dhar
ESTADOS UNIDOS DE AMÉRICA
Address
Aquaculture Pathology Laboratory, School of Animal and Comparative Biomedical Sciences
University of Arizona, 1117 E Lowell St, Building 90, 85721 TucsonContact details
+1-520 621 87.27
[email protected]
Infección por Aphanomyces astaci (plaga del cangrejo de río)
-
Dr. Satu Viljamaa-Dirks
FINLANDIA
Address
Finnish Food Safety Authority
Ruokavirasto Kuopio Neulaniementie 4 70210 Kuopio KUOPIOContact details
+358 447.20.14.69
[email protected]
Infección por Aphanomyces invadans (síndrome ulcerante epizoótico)
-
Dr. Pravata Kumar Pradhan
INDIA
Address
Aquatic Animal Health Laboratory, Exotic & Aquatic Animal Health Division
ICAR-National Bureau of Fish Genetic Resources, Canal Ring Road, P.O. Dilkusha, Lucknow 226 002Contact details
+91522441735
[email protected]
Infección por Bonamia exitiosa
-
Dr. Isabelle Arzul
FRANCIA
Address
IFREMER
Laboratoire de Génétique Aquaculture et Pathologie de Mollusques Marins 17390 La Tremblade La TrembladeContact details
+33 5 46.76.26.10
[email protected]
[email protected]
Infección por Bonamia ostreae
-
Dr. Isabelle Arzul
FRANCIA
Address
IFREMER
Laboratoire de Génétique Aquaculture et Pathologie de Mollusques Marins 17390 La Tremblade La TrembladeContact details
+33 5 46.76.26.10
[email protected]
[email protected]
Infección por Gyrodactylus salaris
-
Dr. Haakon Hansen
NORUEGA
Address
Norwegian Veterinary Institute
Pb 64, N-1431 ÅsContact details
+47-23 21.61.23
[email protected]
[email protected]
Infección por Hepatobacter penaei (hepatopancreatitis necrotizante)
-
Dr Arun Dhar
ESTADOS UNIDOS DE AMÉRICA
Address
Aquaculture Pathology Laboratory, School of Animal and Comparative Biomedical Sciences
University of Arizona, 1117 E Lowell St, Building 90, 85721 TucsonContact details
+1-520 621 87.27
[email protected]
Infección por Marteilia refringens
-
Dr. Isabelle Arzul
FRANCIA
Address
IFREMER
Laboratoire de Génétique Aquaculture et Pathologie de Mollusques Marins 17390 La Tremblade La TrembladeContact details
+33 5 46.76.26.10
[email protected]
[email protected]
Infección por Marteilia sydneyi
-
Dr. Isabelle Arzul
FRANCIA
Address
IFREMER
Laboratoire de Génétique Aquaculture et Pathologie de Mollusques Marins 17390 La Tremblade La TrembladeContact details
+33 5 46.76.26.10
[email protected]
[email protected]
Infección por Megalocytivirus pagrus1
-
Dr. Yasuhiko Kawato
JAPÓN
Address
National Research Institute of AquacultureFisheries Research Agency
422-1 Nakatsuhamaura Minami-ise, Mie 516-0193 MieContact details
+81-599 66.18.30
[email protected]
Infección por Mikrocytos mackini
-
Dr Cathryn Abbot
CANADÁ
Address
Department of Fisheries and Oceans, Pacific Biological Station
3190 Hammond Bay Road, Nanaimo, British Colombia V9T 6N7Contact details
+12506186166
[email protected]
Infección por alfavirus de los salmónidos
-
Dr. Hilde Sindre
NORUEGA
Address
Norwegian Veterinary Institute
Pb 64, N-1431 ÅsContact details
+47 23.21.60.00
[email protected]
[email protected]
Infección por el herpesvirus de la carpa koi
-
Dr. Heike Schutze
ALEMANIA
Address
German Reference Laboratory for Koi Herpesvirus Disease (KHVD)
Institute of Infectology (IMED), Friedrich-Loeffler-Institut (FLI), Federal Research Institute for Animal Health, Institute of Infectology, Südufer 10, 17493 Greifswald – Insel RiemsContact details
+493835171254
[email protected]
-
Dr Takafumi Ito
JAPÓN
Address
Aquaculture Research Department, Fisheries Technology Institute,
Japan Fisheries Research and Education Agency, Nakatsuhamaura 422-1, Minami-ise, Mie 516-0193Contact details
+81599661872
[email protected]
-
Dr. Irene Cano Cejas
REINO UNIDO
Address
The Centre for Environment, Fisheries and Aquaculture Science (CEFAS)Weymouth Laboratory
Barrack Road, The Nothe, Weymouth, Dorset DT4 8UB WeymouthContact details
+44-1305 20.66.42
[email protected]
Infección por el nodavirus Macrobrachium rosenbergii (enfermedad de la cola blanca)
-
Dr. A.Sait Sahul Hameed
INDIA
Address
C.Abdul Hakeem College, Aquatic Animal Health Laboratory, Department of Zoology
Melvisharam-632 509, Ranipet District, Tamil Nadu, Tamil NaduContact details
+91-4172 26.94.87
[email protected]
Infección por el virus de la cabeza amarilla genotipo 1
-
Dr. Nick Moody
AUSTRALIA
Address
CSIRO Australian Centre for Disease Preparedness
5 Portarlington Road, Private Bag 24 (Ryrie Street), Geelong 3220, VictoriaContact details
+61-3 52 27 00 00
[email protected]
Infección por el virus de la necrosis hematopoyética epizoótica
-
Dr. Nick Moody
AUSTRALIA
Address
CSIRO Australian Centre for Disease Preparedness
5 Portarlington Road, Private Bag 24 (Ryrie Street), Geelong 3220, VictoriaContact details
+61-3 52 27 00 00
[email protected]
Infección por el virus de la necrosis hematopoyética infecciosa
-
Dr Kyle Garver
CANADÁ
Address
Pacific Biological Station – Aquatic Animal Health Laboratory (PBS-AAHL)
Fisheries & Oceans Canada, 3190 Hammond Bay Road, Nanaimo V9T 6N7, British ColumbiaContact details
+1-250 756 73 40
[email protected]
-
Dr. Hong Liu
REPÚBLICA POPULAR DE CHINA
Address
Animal and Plant Inspection and Quarantine Technical Center, Shenzhen Customs District
General Administration of Customs, P. R. China (GACC), Building 1011 of Fuqiang Road, Futianqu, Shenzhen, Guangdong Province, 518045Contact details
+86-755 25 58 84 10
[email protected]
[email protected]
Infección por el virus de la necrosis hipodérmica y hematopoyética infecciosa
-
Dr Arun Dhar
ESTADOS UNIDOS DE AMÉRICA
Address
Aquaculture Pathology Laboratory, School of Animal and Comparative Biomedical Sciences
University of Arizona, 1117 E Lowell St, Building 90, 85721 TucsonContact details
+1-520 621 87.27
[email protected]
-
Dr Bing Yang
REPÚBLICA POPULAR DE CHINA
Address
Maricultural Organism Disease Control and Molecular Pathology Laboratory, Yellow Sea Fisheries Research Institute
Chinese Academy of Fishery Sciences, 106 Nanjing Road, Qingdao, Shandong 266071Contact details
+86 532 858 230 62
[email protected]
Infección por el virus de la septicemia hemorrágica viral
-
Dr Kyle Garver
CANADÁ
Address
Pacific Biological Station – Aquatic Animal Health Laboratory (PBS-AAHL)
Fisheries & Oceans Canada, 3190 Hammond Bay Road, Nanaimo V9T 6N7, British ColumbiaContact details
+1-250 756 73 40
[email protected]
-
Dr. Hyoung Jun Kim
COREA (REP. DE)
Address
Pathology Research Division in Aquaculture Research Department
216, Gijanghaean-ro, Gijang-eup, Busan, 46083Contact details
+82-51 720.2114
[email protected]
-
Dr Britt Bang Jansen
DINAMARCA
Address
National Institute for Aquatic Resources
Kemitorvet, Building 202 2800 Kgs, Lyngby LyngbyContact details
+45 35 88 68 31
[email protected]
Infección por el virus de la viremia primaveral de la carpa
-
Dr. Richard Paley
REINO UNIDO
-
Dr. Hong Liu
REPÚBLICA POPULAR DE CHINA
Address
Animal and Plant Inspection and Quarantine Technical Center, Shenzhen Customs District
General Administration of Customs, P. R. China (GACC), Building 1011 of Fuqiang Road, Futianqu, Shenzhen, Guangdong Province, 518045Contact details
+86-755 25 58 84 10
[email protected]
[email protected]
Infección por el virus del síndrome de las manchas blancas
-
Dr Arun Dhar
ESTADOS UNIDOS DE AMÉRICA
Address
Aquaculture Pathology Laboratory, School of Animal and Comparative Biomedical Sciences
University of Arizona, 1117 E Lowell St, Building 90, 85721 TucsonContact details
+1-520 621 87.27
[email protected]
-
Dr. Qingli Zhang
REPÚBLICA POPULAR DE CHINA
Address
Maricultural Organism Disease Control and Molecular Pathology LaboratoryYellow Sea Fisheries Research Institute
Chinese Academy of Fishery Sciences 106 Nanjing Road, Qingdao Shandong 266071 CHINA (PEOPLE'S REP. OF)Contact details
+86 532 858 230 62 ext 812
[email protected]
-
Prof. Han-Ching Wang
TAIPEI CHINO
Address
International Center for the Scientific Development of Shrimp Aquaculture (ICDSA), National Cheng Kung University (NCKU)
No. 500, Sec. 3, Anming Road, Annan District, Tainan City 709Contact details
+886-6 384 24 48
[email protected]
Infección por ranavirus
Infección por virus de la anemia infecciosa del salmón
-
Dr. Sergio Hernán Marshall González
CHILE
Address
Aquaculture Pathology Laboratory,
Pontifical Catholic University of Valparaíso, Curauma Campus, Avenida Universidad 330, ValparaísoContact details
+56322274828
[email protected]
[email protected]
-
Dr. Ole Bendik Dale
NORUEGA
Address
Norwegian Veterinary Institute
Pb 64, N-1431 ÅsContact details
+47-23 21 60 00
[email protected]
[email protected]
Infestación de las abejas melíferas por Aethina tumida (escarabajo de las colmenas)
-
Dr Marc O. Schäfer
ALEMANIA
Address
National Reference Laboratory for Bee Diseases, Friedrich-Loeffer-Institut
Federal Research Institute for Animal Health, Institute of Infectology, Südufer 1017493 Greifswald – Insel RiemsContact details
+49-38351 7 1246
[email protected]
-
Dr Stéphanie Franco
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Sophia Antipolis Laboratory, Honey Bee Pathology Unit, Les Templiers 105 route des Chappes, CS 20111, 06902 Sophia AntipolisContact details
+33 (0)4 92 94 37 00
[email protected]
Infestación de las abejas melíferas por Tropilaelaps spp.
-
Dr Stéphanie Franco
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Sophia Antipolis Laboratory, Honey Bee Pathology Unit, Les Templiers 105 route des Chappes, CS 20111, 06902 Sophia AntipolisContact details
+33 (0)4 92 94 37 00
[email protected]
Influenza aviar
-
Dr Timm C. Harder
ALEMANIA
Address
Friedrich Loeffler InstituteFederal Research Institute for Animal HealthInstitute of Diagnostic Virology
Südufer 10 D-17493 Greifswald Insel Riems GREIFSWALDContact details
+49-38351 7 1152
[email protected]
-
Dr. Frank Wong
AUSTRALIA
Address
CSIRO Australian Centre for Disease Preparedness
5 Portarlington Road, Private Bag 24 (Ryrie Street), Geelong 3220, VictoriaContact details
+61-3 52 27 50 00
[email protected]
[email protected]
-
Dra. Dilmara Reischak
BRASIL
Address
Auditora Fiscal Federal Agropecuária
Laboratório de Diagnóstico Animal, Laboratório Federal de Defesa Agropecuária – LFDA/SP – CGAL, Ministério da Agricultura, Pecuária e Abastecimento, Rua Raul Ferrari, s/n°Jardim Santa Marcelina, CEP 13100-105, Campinas SP, Sao PauloContact details
+551932522117
[email protected]
[email protected]
-
Dr. Yohannes Berhane
CANADÁ
Address
Canadian Food Inspection AgencyNational Centre for Foreign Animal Disease
1015 Arlington Street Winnipeg, Manitoba R3E 3M4 WINNIPEGContact details
+1-204 789 20 03
[email protected]
-
Dr. Eun-Kyoung Lee
COREA (REP. DE)
Address
Animal and Plant Quarantine Agency
Ministry of Agriculture, Forest and Rural Affairs, 177, Hyeoksin 8-ro, Gimcheon-si, Gyeongsangbuk-do 39660Contact details
+82549120968
[email protected]
-
Dr Abdelsatar Arafa
EGIPTO
Address
Reference Laboratory for Veterinary Quality Control on Poultry Production
Animal Health Research Institute, Agriculture research Centre, Ministry of Agriculture and Land Reclamation, 7 Nadi el Seidst. Dokki, GizaContact details
+202-33 37.09.58
[email protected]
-
Dr. Mia Kim Torchetti
ESTADOS UNIDOS DE AMÉRICA
Address
National Veterinary Services Laboratories, USDA, APHIS, VS
1920 Dayton Avenue, Ames, Iowa 50010Contact details
+15153377551
[email protected]
-
Dr. Chakradhar Tosh
INDIA
Address
Indian Council of Agricultural Research (ICAR), National Institute of High Security Animal Diseases (NIHSAD)
Anand Nagar, Bhopal 462 022, Madhya, PradeshContact details
+917552750647
[email protected]
[email protected]
-
Dr Isabella Monne
ITALIA
Address
Istituto Zooprofilattico Sperimentale delle Venezie, Research and Innovation Dept.
Viale Dell'Università 10, 35020 Legnaro PDContact details
+39-049 808 4381
[email protected]
-
Prof. Yoshihiro Sakoda
JAPÓN
Address
Hokkaido University, Research Center for Zoonosis Control
North 20, West 10 Kita-Ku, Sapporo 001-0020Contact details
+81-11 706 52 07
[email protected]
-
Dr. Ashley Banyard
REINO UNIDO
Address
WOAH/FAO International Reference Laboratory for Avian Influenza
Animal and Plant Health Agency – Weybridge, Addlestone, Surrey KT15 3NBContact details
+441483232441
[email protected]
-
Dr Hualan Chen
REPÚBLICA POPULAR DE CHINA
Address
National Avian Influenza Reference Laboratory, Animal Influenza Laboratory of the Ministry of Agriculture
Harbin Veterinary Research Institute, 427 Maduan Street, Harbin 150001Contact details
+86-451 85.93.50.79
[email protected]
-
Dr. Viktor N. Irza
RUSIA
Address
National Reference Laboratory for Avian Influenza and Newcastle Disease
Federal State-Financed Institution “Federal Centre for Animal Health” (FGBI “ARRIAH”), Yur'evets, Vladimir 60090Contact details
+7-4922 26 18 67
[email protected]
[email protected]
Leishmaniosis
-
Dr Fabrizio Vitale
ITALIA
Address
Dept Molecular Biology
Istituto Zooprofilattico Sperimentale della Sicilia (IZSSi), National Reference Centre for Leishmaniasis (C.Re.Na.L.), via Gino Marinuzzi 3, 90129, Palermo PalermoContact details
39-091 656.53.68
[email protected]
Lengua azul
-
Dr Debbie Eagles
AUSTRALIA
Address
CSIRO
5 Portarlington Road, Private Bag 24 (Ryrie Street), Geelong 3220, VictoriaContact details
+61-3 52 27 00 00
[email protected]
-
Dr Giovanni Savini
ITALIA
Address
Istituto Zooprofilattico Sperimentale dell'Abruzzo e del Molise "G. Caporale"
Via Campo Boario, 64100 TeramoContact details
+39-0861 33 24 40
[email protected]
-
Dr. Carrie Batten
REINO UNIDO
Address
Pirbright
Ash Road, Woking, Surrey GU24 0NFContact details
+44-1483 23 24 41
[email protected]
-
Dr Baratang Alison Lubisi
SUDÁFRICA
Address
Senior Research Veterinarian
Onderstepoort Veterinary Institute, Agricultural Research Council, Private Bag X05, Onderstepoort 0110Contact details
+27-12 529 91 17
[email protected]
Leptospirosis
-
Dra. Jessica Petrakovsky
ARGENTINA
Address
Laboratorio de Leptospirosis, Dirección General de Laboratorios y Control Técnico, Servicio Nacional de Sanidad y Calidad Agroalimentaria (SENASA)
Avenida Talcahuano N° 1660 (1640), Martínez, Pcia de Buenos AiresContact details
+54-11 48.36.11.14 int 287 o 299
[email protected]
-
Dr. Luis Samartino
ARGENTINA
Address
CICVyA INTA, Instituto de Bacteriología
Casilla de Correo 25, Castelar 1712, Moron, Provincia de Buenos AiresContact details
+541146211289
[email protected]
-
Dr. Matthew Erdman
ESTADOS UNIDOS DE AMÉRICA
Address
USDA APHIS Veterinary Services, Diagnostics and Biologics
1910 Dayton Ave, Ames, IA 50010 UNITED STATES OF AMERICAContact details
+15153377200
[email protected]
[email protected]
[email protected]
-
Dr. Vinayagamurthy Balamurugan
INDIA
Address
Indian Council of Agricultural Research-National Institute of Veterinary Epidemiology and Disease Informatics (ICAR-NIVEDI)
Yelahanka, Bengaluru-560064, KarnatakaContact details
+9108023093136
[email protected]
[email protected]
-
Dr. Paula Ristow
PAÍSES BAJOS
Address
Academic Medical Center, Department of Medical Microbiology and Infection Prevention
University of Amsterdam, Meibergdreef 39, 1105 AZ AmsterdamContact details
+31205665431
[email protected]
[email protected]
Leucosis bovina enzoótica
-
Dr. Jacek Kuzmak
POLONIA
Address
National Veterinary Research Institute
Al. Partyzantow str. 57 24-100 Pulawy PulawyContact details
+48-81 889.31.14
[email protected]
-
Dr Bhudipa Choudhury
REINO UNIDO
Address
Animal and Plant Health Agency
New Haw, Addlestone, Weybridge, Surrey KT15 3NBContact details
+44-1932 35.75.59
[email protected]
Loque americana (infección de las abejas melíferas por Paenibacillus larvae)
-
Dr Marc O. Schäfer
ALEMANIA
Address
National Reference Laboratory for Bee Diseases, Friedrich-Loeffer-Institut
Federal Research Institute for Animal Health, Institute of Infectology, Südufer 1017493 Greifswald – Insel RiemsContact details
+49-38351 7 1246
[email protected]
-
Dr Marie-Pierre Chauzat
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Sophia Antipolis Laboratory, Honey Bee Pathology Unit, Les Templiers 105 route des Chappes, CS 20111, 06902 Sophia AntipolisContact details
+33 (0)4 92 94 37 00
[email protected]
-
Dr. Richard J. Hall
NUEVA ZELANDA
Address
Animal Health Laboratory
Diagnostic and Surveillance Services, Biosecurity New Zealand, Ministry for Primary Industries, 66 Ward Street, Wallaceville, Upper Hutt 5018Contact details
+6448945600
[email protected]
Loque europea (infección de las abejas melíferas por Melissococcus plutonius)
-
Dr Marie-Pierre Chauzat
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Sophia Antipolis Laboratory, Honey Bee Pathology Unit, Les Templiers 105 route des Chappes, CS 20111, 06902 Sophia AntipolisContact details
+33 (0)4 92 94 37 00
[email protected]
Metritis contagiosa equina
-
Dr. Kristina Lantz
ESTADOS UNIDOS DE AMÉRICA
-
Dr Sandrine Petry
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Animal Health Laboratory (Normandy site), Physiopathology and Epidemiology of Equine Diseases Unit, 14430 DozuléContact details
+330231797971
[email protected]
-
Dr. Ian Mawhinney
REINO UNIDO
Address
Animal and Plant Health Agency Bury St Edmunds
Rougham Hill, Bury St Edmunds, Suffolk IP44 2RXContact details
+441284724499
[email protected]
Miasis por Cochliomyia hominivorax
-
To Be Decided
PANAMÁ
Address
Panama–United States Commission for the Eradication and Prevention of Screwworm (COPEG)
Screwworm Fly Production Plant, P.O. Box 0816-07636, Panama CityContact details
+5072960006
[email protected]
[email protected]
Micoplasmosis aviar (Mycoplasma gallisepticum)
-
Dr. Salvatore Catania
ITALIA
Address
Avian Medicine Laboratory, Mycoplasma Unit
Istituto Zooprofilattico Sperimentale delle Venezie, Via Bovolino 1/CContact details
+39045500285
[email protected]
-
Dr. Umit Sevimli
REPÚBLICA DE TÜRKIYE
Address
Pandik Veterinary Control Institute
Batı mahallesi, Erol Kaya caddesi 1, 34890 İstanbulContact details
+90-216 390.12.80
[email protected]
[email protected]
Micoplasmosis aviar (Mycoplasma synoviae)
-
Dr. Salvatore Catania
ITALIA
Address
Avian Medicine Laboratory, Mycoplasma Unit
Istituto Zooprofilattico Sperimentale delle Venezie, Via Bovolino 1/CContact details
+39045500285
[email protected]
-
Dr. Umit Sevimli
REPÚBLICA DE TÜRKIYE
Address
Pandik Veterinary Control Institute
Batı mahallesi, Erol Kaya caddesi 1, 34890 İstanbulContact details
+90-216 390.12.80
[email protected]
[email protected]
Mixomatosis
-
Dr. Antonio Lavazza
ITALIA
Address
Dept. Animal Health and Welfare
Via Antonio Bianchi 9, 25124 BresciaContact details
+39-030 22.90.617
[email protected]
Muermo
-
Dr. Heinrich Neubauer
ALEMANIA
Address
Institute of Bacterial Infections and Zoonoses, Friedrich-Loeffer Institute,
Naumburger Str. 96a, 07743 JenaContact details
+49-3641 804 2100
[email protected]
[email protected]
[email protected]
-
Prof. Ulrich Wernery
EMIRATOS ÁRABES UNIDOS
Address
Central Veterinary Research Laboratory
P.O. Box 597 Dubai DubaiContact details
+971-4 337.51.65
[email protected]
-
Dr Karine Laroucau
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Animal Health Laboratory (Maisons-Alfort), Bacterial Zoonoses Unit, 14 rue Pierre et Marie Curie, 94701 Maisons-Alfort CedexContact details
+330149771350
[email protected]
Nagana (tripanosomiasis africana animal transmitida por la mosca tsetsé)
-
Dr. Marc Desquesnes
FRANCIA
Address
UMR177-Intertryp (CIRAD-IRD)CIRAD-bios
Campus international de Baillarguet TA A-17 / G 34398 Montpellier Cedex 5 MontpellierContact details
+33-(0)4 67 59 37 24
[email protected]
Nosemosis de las abejas melíferas
-
Dr Marie-Pierre Chauzat
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Sophia Antipolis Laboratory, Honey Bee Pathology Unit, Les Templiers 105 route des Chappes, CS 20111, 06902 Sophia AntipolisContact details
+33 (0)4 92 94 37 00
[email protected]
Paratuberculosis
-
Dr Bernardo Alonso
ARGENTINA
Address
DILAB (Dirección de Laboratorios y Control Técnico) Servicio Nacional de Sanidad y Calidad, Agroalimentaria (SENASA)
Talcahuano 1660,1640 Martínez, Prov. de Buenos AiresContact details
+54-11 48.74.67.35
[email protected]
[email protected]
-
Dr Virginie Poisson
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Ploufragan-Plouzané- Niort Laboratory, 60 rue de Pied-de-Fond, CS 28440, 79024 Niort CedexContact details
+33 (0)5 49.79.61.28
[email protected]
-
Dr. Matteo Ricchi
ITALIA
Address
National Reference Centre for Paratuberculosis
Istituto Zooprofilattico Sperimentale della Lombardia e dell’Emilia Romagna, Sede Territoriale di Piacenza, Strada della Faggiola 1, 29027 Gariga di Podenzano (PC)Contact details
+390523524253
[email protected]
[email protected]
Perineumonía contagiosa bovina
-
To Be Decided
BOTSUANA
Address
National Veterinary Laboratory
Private Bag 0035, GaboroneContact details
+267 392 87 16
[email protected]
-
Dr Lucia Manso-Silvan
FRANCIA
Address
CIRAD Département BIOSUMR CIRAD-INRAe ASTRE : "Animal, Santé, Territoires, Risques, Ecosystèmes"
Campus International de Baillarguet TA A-117/E 34398 Montpellier Cedex 5 MONTPELLIERContact details
+33 (0)4 67 59 37 39
[email protected]
-
Dr. Massimo Scacchia
ITALIA
Address
Istituto Zooprofilattico Sperimentaledell'Abruzzo e del Molise 'G. Caporale'
Via Campo Boario 64100 Teramo TERAMOContact details
+390-861 33 24 05
[email protected]
-
Dr Ana Rosa Pombo Botelho
PORTUGAL
Address
Instituto Nacional de Investigação Agrária e Veterinária (INIAV, IP)
Av. da República, Quinta do Marquês, s/n 2780-157 Oeiras OEIRASContact details
+351-21 440 35 14
[email protected]
Peste bovina
-
Dr. Wei Jia
ESTADOS UNIDOS DE AMÉRICA
Address
National Veterinary Services Laboratories, USDA, APHIS, VS
40550 Route 25, Orient, New York, NY 11957Contact details
+16313233197
[email protected]
-
Dr. Arnaud Bataille
FRANCIA
Address
CIRAD-Bios
Campus International de Baillarguet TA A-15/G, 34398 Montpellier Cedex 5Contact details
+33 (0)4 67 59 37 98
[email protected]
-
Dr Takehiro Kokuho
JAPÓN
Address
Exotic Disease Research DivisionNational Institute of Animal Health (NIAH)
National Agriculture and Food Research Organization (NARO) Josuihoncho 6-20-1 Kodaira Tokyo, 187-0022 TokyoContact details
+81-42 321.14 66
[email protected]
-
Dr Michael Baron
REINO UNIDO
Address
Ash Road, Pirbright Woking, Surrey, GU24 0NFContact details
+44-1483 23.24.41
[email protected]
Peste de peque~nos rumiantes
-
Dr. Arnaud Bataille
FRANCIA
Address
CIRAD-Bios
Campus International de Baillarguet TA A-15/G, 34398 Montpellier Cedex 5Contact details
+33 (0)4 67 59 37 98
[email protected]
-
Dr. Vinayagamurthy Balamurugan
INDIA
Address
Indian Council of Agricultural Research-National Institute of Veterinary Epidemiology and Disease Informatics (ICAR-NIVEDI)
Yelahanka, Bengaluru-560064, KarnatakaContact details
+9108023093136
[email protected]
[email protected]
-
Dr Michael Baron
REINO UNIDO
Address
Ash Road, Pirbright Woking, Surrey, GU24 0NFContact details
+44-1483 23.24.41
[email protected]
-
Zhiliang Wang
REPÚBLICA POPULAR DE CHINA
Address
National Surveillance and Research Center for Exotic Animal Diseases
China Animal Health and Epidemiology Center, 369 Nanjing Road, Qingdao 266032Contact details
+8653285639166
[email protected]
[email protected]
Peste equina
-
Dr Montserrat Agüero Garcia
ESPAÑA
Address
Laboratorio Central de Sanidad Animal
LCV-Algete, Ctra. Algete Km 828110 Algete, MadridContact details
+34 913 47 83 12
[email protected]
-
Dr. Carrie Batten
REINO UNIDO
Address
Pirbright
Ash Road, Woking, Surrey GU24 0NFContact details
+44-1483 23 24 41
[email protected]
-
Dr Baratang Alison Lubisi
SUDÁFRICA
Address
Senior Research Veterinarian
Onderstepoort Veterinary Institute, Agricultural Research Council, Private Bag X05, Onderstepoort 0110Contact details
+27-12 529 91 17
[email protected]
Peste porcina africana
-
Dr David Williams
AUSTRALIA
Address
CSIRO Australian Centre for Disease Preparedness
5 Portarlington Road, Geelong, Victoria 3220Contact details
+61 52.27.50.00
[email protected]
-
Dr Aruna Ambagala
CANADÁ
Address
National Centre for Foreign Animal Disease, Canadian Food Inspection Agency
1015 Arlington Street, Winnipeg, Manitoba R3E 3M4Contact details
+12047892089
[email protected]
[email protected]
-
Dra. María del Carmen Gallardo Frontaura
ESPAÑA
Address
Centro de Investigación en Sanidad Animal (CISA)/Instituto Nacional de Investigación y Tecnología Agraria y Alimentaria (INIA) del Consejo Superior de Investigaciones Científicas (CSIC)
Carretera Algete-El Casar de Talamanca, Km. 8,1, 28130 Valdeolmos, MadridContact details
+34916292300
[email protected]
-
Dr. Ping Wu
ESTADOS UNIDOS DE AMÉRICA
Address
National Veterinary Services Laboratories, USDA, APHIS, VS
40550 Route 25, Orient, New York, NY 11957Contact details
+16313233287
[email protected]
-
Dr. Christopher Netherton
REINO UNIDO
Address
The Pirbright Institute
Ash Road, Pirbright, Woking, Surrey GU24 0NFContact details
+441483232441
[email protected]
-
Dr. Xiaodong Wu
REPÚBLICA POPULAR DE CHINA
Address
National ASF Reference Laboratory,
China Animal Health and Epidemiology Center, Qingdao 266032,Contact details
+8653213706428161
[email protected]
-
Dr Livio Heath
SUDÁFRICA
Address
Onderstepoort Veterinary Institute,
Agricultural Research Council, Private Bag X05, Onderstepoort 0110Contact details
+27-12 529 95.01
[email protected]
Peste porcina clásica
-
Prof. Paul Becher
ALEMANIA
Address
University of Veterinary Medicine of Hannover Department of Infectious DiseasesInstitute of Virology
Bünteweg 17 30559 Hannover HANOVREContact details
+49-511 953 88 40
[email protected]
-
Dr Aruna Ambagala
CANADÁ
Address
National Centre for Foreign Animal Disease, Canadian Food Inspection Agency
1015 Arlington Street, Winnipeg, Manitoba R3E 3M4Contact details
+12047892089
[email protected]
[email protected]
-
Dra. Llilianne Ganges
ESPAÑA
Address
Institut de Recerca i Tecnologia Agroalimentàries (IRTA)
Centre de Recerca en Sanitat Animal (CReSA), Edifici CreSA, Campus de la Universidad Autónoma de Barcelona, Bellaterra 08193 (Barcelona)Contact details
+34-934 67 40 40 ext. 1786
[email protected]
-
Dr. Katsuhiko Fukai
JAPÓN
Address
National Institute of Animal HealthDepartment of Exotic Diseases
6-20-1 Josui-Honcho Kodaira Tokyo 187-0022 TOKYOContact details
+81-42 321 14 41
[email protected]
-
Dr. Katarzyna Podgórska
POLONIA
Address
National Veterinary Research Institute
Partyzantow Str. 5724-100 PulawyContact details
+48-81 889 30 47
[email protected]
[email protected]
-
Dr Helen Crooke
REINO UNIDO
Address
Animal and Plant Health Agency
New Haw, Addlestone, Weybridge, Surrey KT15 3NBContact details
+44-208 026 9665
[email protected]
-
Prof. Qin Wang
REPÚBLICA POPULAR DE CHINA
Address
China Institute of Veterinary Drug Control (IVDC)/Center for Veterinary Drug Evaluation (CVDE)
Department of Reference Substance Research, No.8 Zhongguancun South Street, Haidian District, Beijing 100081Contact details
+86-010 612 55 400
[email protected]
[email protected]
[email protected]
-
Dr. Yu-Liang Huang
TAIPEI CHINO
Address
Veterinary Research Institute, Council of Agriculture
376 Chung-Cheng Rd, Tamsui District, New Taipei City 25158Contact details
+886226212111
[email protected]
Piroplasmosis equina
-
Dr. Sanjay Kumar
INDIA
Address
Equine Piroplasmosis Laboratory
Indian Council of Agricultural Research-National Research Center on Equines (ICAR-NRCE),Sirsa Road, Hisar 125 001, HaryanaContact details
+911662282503
[email protected]
-
Prof. Naoaki Yokoyama
JAPÓN
Address
Obihiro University of Agriculture and Veterinary Medicine
Obihiro University of Agriculture and Veterinary Medicine Nishi 2-13, Inada-cho Obihiro, Hokkaido 080-8555 HokkaidoContact details
+81-155 49.56.49
[email protected]
Pleuroneumonía contagiosa caprina
-
Dr Lucia Manso-Silvan
FRANCIA
Address
CIRAD Département BIOSUMR CIRAD-INRAe ASTRE : "Animal, Santé, Territoires, Risques, Ecosystèmes"
Campus International de Baillarguet TA A-117/E 34398 Montpellier Cedex 5 MONTPELLIERContact details
+33 (0)4 67 59 37 39
[email protected]
-
Dr. Umit Sevimli
REPÚBLICA DE TÜRKIYE
Address
Pandik Veterinary Control Institute
Batı mahallesi, Erol Kaya caddesi 1, 34890 İstanbulContact details
+90-216 390.12.80
[email protected]
[email protected]
Prurigo lumbar
-
Dr. Gordon Mitchell
CANADÁ
Address
Canadian Food Inspection Agency, Ottawa Laboratory (Fallowfield), Animal Disease Research Institute
3851 Fallowfield Road, P.O. Box 11300, Station H, Nepean, Ontario K2H 8P9nContact details
+1-613 221.48.54
[email protected]
-
Dr Juan José Badiola Díez
ESPAÑA
Address
Centro de investigación en Encefalopatías y enfermedades transmisibles emergentes
Universidad de Zaragoza, Facultad de Veterinaria, Departamento de Patología Animal, Miguel Servet 177, 50013 ZaragozaContact details
+34-976 76 20 19
[email protected]
-
Dr. Cristina Casalone
ITALIA
Address
Italian National Reference Centre for Diagnostic Activities in Stranded Marine Mammals (C.Re.Di.Ma.), via Bologna 148, 10154 TorinoContact details
+39-11 26 86 296
[email protected]
[email protected]
-
Dr. John Spiropoulos
REINO UNIDO
Address
Animal and Plant Health Agency
New Haw, Addlestone, Weybridge, Surrey KT15 3NBContact details
+44 1932 357.564
[email protected]
-
Prof. Torsten Seuberlich
SUIZA
Address
Neuro Centre Department of Clinical Research and Veterinary Public Health
Division of Experimental Clinical Research, University of Bern, Bremgartenstrasse 109 A3012 Bern,Contact details
+41-31 631 22 06
[email protected]
Rabia
-
Dr Thomas Müller
ALEMANIA
Address
Institute of Molecular Virology and Cell Biology, Friedrich-Loeffler Institut,Federal Research Institute for Animal Health
Südufer 10 D-17493 Greifswald – Insel Riems GreifswaldContact details
+49-38351 7 1659
[email protected]
-
Dr. Christine Fehlner-Gardiner
CANADÁ
Address
Centre of Expertise for Rabies CFIA/ACIA, Ottawa Laboratory Fallowfield, Animal Diseases Research Institute
3851 Fallowfield Road, P.O. Box 11300, Station H, Nepean, Ontario K2H 8P9Contact details
+1-343 212 03 04
[email protected]
-
Dr. Dong-Kun Yang
COREA (REP. DE)
Address
Animal and Plant Quarantine Agency
177 Hyeoksin 8-ro Gimcheong-si Gyeongsangbuk-do 39660 GyeongsangbukContact details
+82 31 467.1783
[email protected]
-
Dr. Ryan Wallace
ESTADOS UNIDOS DE AMÉRICA
Address
Poxvirus and Rabies Branch, Division of High-Consequence Pathogens and Pathology
National Center for Emerging and Zoonotic Infectious Diseases, Centers for Disease Control and Prevention, 1600 Clifton Road, NE, Mail Stop G33, Atlanta, GA 30 333Contact details
+1-404 639.10.50
[email protected]
-
Dr Florence Cliquet
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Laboratory for Rabies and Wildlife (Nancy), Technopôle agricole et vétérinaire Domaine de Pixérécourt, B.P. 40009, 54220 Malzéville CedexContact details
+33 (0)3 83 29 89 50
[email protected]
-
Dr Shrikrishna Isloor
INDIA
Address
OIE Twinned KVAFSU-CVA Rabies Diagnostic Laboratory, Department of Microbiology, Veterinary College
Karnataka Veterinary, Animal and Fisheries Sciences University (KVAFSU), Hebbal, Bangalore 560024,Contact details
+91-80 29.53.22.87
[email protected]
-
Dr Boris Yakobson
ISRAEL
Address
Kimron Veterinary Institute
Veterinary Services and Animal Health, P.O. Box 12, Beit Dagan 50250Contact details
+ 972-3 9681720
[email protected]
-
Dr. Paola De Benedictis
ITALIA
Address
Laboratory for Emerging Viral Zoonoses, Research and Innovation Department
Istituto Zooprofilattico Sperimentale Delle Venezie, Viale dell’Università 10, 35020 Legnaro (PD)Contact details
+390498084385
[email protected]
-
Dr. Juan Antonio Montaño Hirose
MÉXICO
Address
Centro Nacional de Servicios de Diagnóstico en Salud Animal
Av. Centenario de la Educación s/n (Km 37.5 Carretera Federal México – Pachuca) 55740 Tecámac de Felipe Villanueva Tecámac, Estado de México TecámacContact details
+525559051000
[email protected]
[email protected]
-
Dr Anthony Fooks
REINO UNIDO
Address
Animal and Plant Health Agency
New Haw, Addlestone, Weybridge, Surrey KT15 3NBContact details
+44-208 415.22.38
[email protected]
-
Prof. Changchun Tu
REPÚBLICA POPULAR DE CHINA
Address
Diagnostic Laboratory for Rabies and Wildlife Associated Zoonoses, Department of Virology, Changchun Veterinary Research Institute (CVRI),
Chinese Academy of Agricultural Sciences (CAAS), 573 Yujinxiang Street, Jingyue Economic Development Zone, Changchun 130122Contact details
+86-431 81.03.20.22
[email protected]
-
Dr Vlad Vuta
RUMANIA
Address
National Reference Laboratory for Rabies, Institute for Diagnosis and Animal Health
Dr Nicolae Staicovici Street, No. 63, Sector 5, Bucharest 050557Contact details
+40-374 32.20.00
[email protected]
[email protected]
-
Dr Claude Taurai Sabeta
SUDÁFRICA
Address
Rabies Unit
Onderstepoort Veterinary Institute, Agricultural Research Council, Private Bag X05, Onderstepoort 0110Contact details
+27-12 529 94 39
[email protected]
-
Dr. Ai-Ping Hsu
TAIPEI CHINO
Address
Veterinary Research Institute, Ministry of Agriculture
No. 376, Zhongzheng Rd., Tamsui Dist., New Taipei City 251018Contact details
+886226212111
[email protected]
Resistencia microbiana
-
Dr Chris Teale
REINO UNIDO
Address
Animal and Plant Health Agency
New Haw, Addlestone, Weybridge, Surrey KT15 3NBContact details
+44-1743 46 76 21
[email protected]
Rinoneumonía equina
-
Dr. Lutz Goehring
ESTADOS UNIDOS DE AMÉRICA
Address
Department of Veterinary Science
Maxwell H. Gluck Equine Research Center, University of Kentucky, 108 Gluck Equine Research Center Lexington, Kentucky 40546-0099Contact details
+18592574757
[email protected]
-
Prof. Ann Cullinane
IRLANDA
Address
Irish Equine Centre
Johnstown, Naas, Co. KildareContact details
+353-45 86.62.66
[email protected]
-
Dr. Hiroshi Bannai
JAPÓN
Address
Equine Research Institute, Japan Racing Association
1400-4 Shiba, Shimotsuke, Tochigi 329-0412Contact details
+81285440090
[email protected]
Rinotraqueítis del pavo
-
Dr Nicolas Eterradossi
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Ploufragan-Plouzané-Niort Laboratory, Poultry and Rabbit Virology, Immunology, Parasitology Unit, B.P. 53, 22440 PloufraganContact details
+33 (0)2 96 01 62 22
[email protected]
Rinotraqueítis infecciosa bovina/vulvovaginitis pustular infecciosa
-
Dr. Martin Beer
ALEMANIA
Address
Institute of Diagnostic VirologyFriedrich-Loeffler Institut,Federal Research Institute for Animal Health
Südufer 10 D-17493 Greifswald, Insel RiemsContact details
+49 38351 7 1223
[email protected]
-
Dr Akbar Dastjerdi
REINO UNIDO
Address
Animal and Plant Health Agency
New Haw, Addlestone, Weybridge, Surrey KT15 3NBContact details
+44-1932 35.75.08
[email protected]
Salmonelosis
-
Dr. Istvan Szabo
ALEMANIA
Address
Federal Institute for Risk Assessment
Diedersdorfer Weg 1 D-12277 Berlin BERLINContact details
+49-30 184 12 22 20
[email protected]
-
Dr. Gitanjali Arya
CANADÁ
Address
The Guelph Reference Services Unit, The National Microbiology Laboratory at Guelph
Public Health Agency of Canada, 110 Stone Road West, Guelph, ON N1G 3W4Contact details
+15198262640
[email protected]
-
Dr. Min-Su Kang
COREA (REP. DE)
Address
Avian Bacteriology LaboratoryAvian Disease Research Division
Animal and Plant Quarantine Agency (APQA) Ministry of Agriculture, Food and Rural Affairs (MAFRA) 177, Hyeoksin 8-ro Gimcheon-si Gyeongsangbuk-do, 39660, Gimcheon-siContact details
+82-54 912 08 18
[email protected]
-
Dr. Antonia Ricci
ITALIA
Address
Istituto Zooprofilattico Sperimentale delle Venezie, National Reference Laboratory for Salmonella
Viale dell'Università, 10,35020 Legnaro (Padova), LegnaroContact details
+39-049 8084.296
[email protected]
-
Dr. Renatus Peter Shilangale
NAMIBIA
Address
Central Veterinary Laboratory
Ministry of Agriculture, Water and Land Reform, 24 Goethe Street, P-Bag 13187, WindhoekContact details
+26461237684
[email protected]
[email protected]
-
Dr. Francesca Martelli
REINO UNIDO
Septicemia entérica del bagre (Edwardsiella ictaluri)
-
Dr Larry A. Hanson
ESTADOS UNIDOS DE AMÉRICA
Address
Fish Diagnostic Laboratory, College of Veterinary Medicine, Mississippi State University
P.O. Box 6100, Spring Street, Mississippi 39762Contact details
+1-662 325 12 02
[email protected]
Surra (Trypanosoma evansi)
-
Dr. Nick Van Reet
BÉLGICA
Address
Institute of Tropical Medicine AntwerpDepartment of Parasitology
Nationalestraat 155B-2000 AntwerpenContact details
+32-3 247.63.71
[email protected]
-
Prof. Noboru Inoue
JAPÓN
Address
National Research Center for Protozoan DiseasesObihiro University of Agricultureand Veterinary Medicine
Inada-cho Nishi 2-13 Obihiro, Hokkaido 080-8555 HokkaidoContact details
+81-155 49.56.47
[email protected]
Síndrome disgenésico y respiratorio porcino
-
Dr. Katarzyna Podgórska
POLONIA
Address
National Veterinary Research Institute
Partyzantow Str. 5724-100 PulawyContact details
+48-81 889 30 47
[email protected]
[email protected]
-
Dr. Kegong Tian
REPÚBLICA POPULAR DE CHINA
Address
Veterinary Diagnostic LaboratoryChina Animal Disease Control Center
No.17 Tiangui Street Biomedical Base Daxing District Beijing 102618 BeijingContact details
+86-10 59.19.88.96
[email protected]
[email protected]
Síndrome respiratorio de Oriente Medio
-
Prof. Ulrich Wernery
EMIRATOS ÁRABES UNIDOS
Address
Central Veterinary Research Laboratory
P.O. Box 597 Dubai DubaiContact details
+971-4 337.51.65
[email protected]
Teileriosis
-
To Be Decided
ITALIA
Address
Istituto Zooprofilattico Sperimentale della Sicilia (IZSSi),
Italian Reference Centre for Anaplasma, Babesia, Rickettsia, Theileria (C.R.A.Ba.R.T.), via Gino Marinuzzi 3, 90129, PalermoContact details
+39-091 656.53.41 ext 219
[email protected]
-
Dr. Barend Johannes Mans
SUDÁFRICA
Address
Epidemiology, Parasites and Vectors
Agricultural Research Council, Onderstepoort Veterinary Research, Onderstepoort 0110Contact details
+27125299200
[email protected]
Teileriosis ovina
-
Prof. Hong Yin
REPÚBLICA POPULAR DE CHINA
Address
Lanzhou Veterinary Research Institute, Chinese Academy of Agricultural Sciences(CAAS)
Vector and Vector and Vector-borne Diseases Control Laboratory (VVBDC), Xujiaping 1, Chengguan District, Lanzhou, Gansu Province 730046Contact details
+86-93 18.34.26.81
[email protected]
Tripanosomosis (transmitida por tsetsé)
-
Dr. Marc Desquesnes
FRANCIA
Address
UMR177-Intertryp (CIRAD-IRD)CIRAD-bios
Campus international de Baillarguet TA A-17 / G 34398 Montpellier Cedex 5 MontpellierContact details
+33-(0)4 67 59 37 24
[email protected]
Triquinelosis
-
To Be Decided
CANADÁ
Address
Canadian Food Inspection Agency
Canadian Food Inspection Agency, 116 Veterinary Road, Saskatoon, Saskatchewan S7N 2R3Contact details
+13063857815
[email protected]
-
Dr. Gianluca Marucci
ITALIA
Address
Istituto Superiore di Sanita, Dipartimento di Malattie Infettive
Viale Regina Elena 299, 00161 RomaContact details
+390649902310
[email protected]
Tuberculosis de los mamíferos
-
Dr Bernardo Alonso
ARGENTINA
Address
DILAB (Dirección de Laboratorios y Control Técnico) Servicio Nacional de Sanidad y Calidad, Agroalimentaria (SENASA)
Talcahuano 1660,1640 Martínez, Prov. de Buenos AiresContact details
+54-11 48.74.67.35
[email protected]
[email protected]
-
Dra. Beatriz ROMERO MARTINEZ
ESPAÑA
Address
Centro de Vigilancia Sanitaria Veterinaria (VISAVET)
VISAVET Health Surveillance Centre, Universidad Complutense Madrid, Avenida Puerta de Hierro s/n, 28040 MadridContact details
+34913944033
[email protected]
[email protected]
-
Dr. Tyler C. Thacker
ESTADOS UNIDOS DE AMÉRICA
Address
National Veterinary Services Laboratories, USDA, APHIS, VS
1920 Dayton Avenue, Ames, Iowa 50010Contact details
+15153377034
[email protected]
-
Dr María Laura Boschiroli-Cara
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Animal Health Laboratory (Maisons-Alfort), Bacterial Zoonoses Unit, 14 rue Pierre et Marie Curie, 94701 Maisons-Alfort CedexContact details
+330149771350
[email protected]
-
Dr Jason Sawyer
REINO UNIDO
Address
Animal and Plant Health Agency
New Haw, Addlestone, Weybridge, Surrey KT15 3NBContact details
+44-1932 34.11.11
[email protected]
Tularemia
-
Dr. Herbert Tomaso
ALEMANIA
Address
Institute for Bacterial Infections and Zoonoses, Friedrich-Loeffler-Institut (FLI)
Naumburger Str. 96a – 07743 JenaContact details
+4936418042243
[email protected]
Varroosis (infestación de las abejas melíferas por Varroa spp.)
-
Dr Marc O. Schäfer
ALEMANIA
Address
National Reference Laboratory for Bee Diseases, Friedrich-Loeffer-Institut
Federal Research Institute for Animal Health, Institute of Infectology, Südufer 1017493 Greifswald – Insel RiemsContact details
+49-38351 7 1246
[email protected]
-
Dr Marie-Pierre Chauzat
FRANCIA
Address
ANSES (French Agency for Food, Environmental and Occupational Health & Safety)
Sophia Antipolis Laboratory, Honey Bee Pathology Unit, Les Templiers 105 route des Chappes, CS 20111, 06902 Sophia AntipolisContact details
+33 (0)4 92 94 37 00
[email protected]
-
Dr. Richard J. Hall
NUEVA ZELANDA
Address
Animal Health Laboratory
Diagnostic and Surveillance Services, Biosecurity New Zealand, Ministry for Primary Industries, 66 Ward Street, Wallaceville, Upper Hutt 5018Contact details
+6448945600
[email protected]
Virosis del bagre de canal
-
Dr Larry A. Hanson
ESTADOS UNIDOS DE AMÉRICA
Address
Fish Diagnostic Laboratory, College of Veterinary Medicine, Mississippi State University
P.O. Box 6100, Spring Street, Mississippi 39762Contact details
+1-662 325 12 02
[email protected]
Viruela del camello
-
Prof. Ulrich Wernery
EMIRATOS ÁRABES UNIDOS
Address
Central Veterinary Research Laboratory
P.O. Box 597 Dubai DubaiContact details
+971-4 337.51.65
[email protected]
Viruela ovina y viruela caprina
-
Dr. Nick De Regge
BÉLGICA
Address
Department of Infectious Diseases in Animals
Exotic and vector-borne diseases (EXOVEC), Sciensano, Groeselenberg 99, 1180 UccleContact details
+3223790514
[email protected]
-
Dr. Mohammad Hassan Ebrahimi-jam
IRÁN
Address
RAZI Vaccine & Serum Research Institute
Karaj 3197619751, Teheran,Contact details
+982634570038
[email protected]
[email protected]
-
Georgina Limon-Vega
REINO UNIDO
Address
Pirbright,
Ash Road, Woking, Surrey GU24 0NFContact details
+44-1483 23.24.41
[email protected]
-
Dr Baratang Alison Lubisi
SUDÁFRICA
Address
Senior Research Veterinarian
Onderstepoort Veterinary Institute, Agricultural Research Council, Private Bag X05, Onderstepoort 0110Contact details
+27-12 529 91 17
[email protected]
Virus iridiscente de los decápod 1
-
Dr. Liang Qiu
REPÚBLICA POPULAR DE CHINA
Address
Division of Maricultural Organism, Disease Control and Molecular Pathology
Yellow Sea Fisheries Research Institute (YSFRI), Chinese Academy of Fishery Sciences, #106 Nanjing Road, Qingdao, Shandong Province 266071Contact details
+8653285823062
[email protected]
-
Dr. Chien Tu
TAIPEI CHINO
Address
Aquatic Medicine Laboratory, Biology Division, Animal Health Research Institute (AHRI), Council of Agriculture
376 Chung-Cheng Road, Tamsui, New Taipei City 25158Contact details
+886226212111
[email protected]
[email protected]
Evaluación de la Capacidad de los Laboratorios
1. Introducción
1.1. Objetivos
El presente documento formula directrices para la evaluación de la aptitud de los laboratorios para efectuar pruebas de diagnóstico de enfermedades infecciosas.
1.2. Aplicación
Estas directrices están destinadas a los Países Miembros de la OMSA para que las apliquen en la evaluación de los laboratorios que examinan animales y productos de origen animal destinados al transporte internacional. Deben ser utilizadas junto con las directrices de la OMSA para evaluar la calidad de los laboratorios a fin de valorar la capacidad y calidad general de los laboratorios.
La presente guía se ajusta a los requisitos generales de la serie de normas ISO[1]9000,
ISO/IEC[2]17025 y la Guía 43 de ISO.
1.3. Comparaciones entre laboratorios
Las comparaciones entre laboratorios se pueden emprender por diversos motivos, entre ellos:
i) determinar la aptitud de un laboratorio para realizar pruebas de diagnóstico específicas;
ii) verificar o certificar el desempeño de determinados técnicos;
iii) verificar o certificar la calibración del instrumental;
iv) armonizar los métodos de análisis existentes;
v) evaluar nuevos métodos de prueba;
vi) asignar valores y límites de fluctuación aceptables para material normalizado;
vii) resolver diferencias entre laboratorios.
1.4. Evaluación de la idoneidad
Cuando una comparación entre laboratorios se realiza expresamente para determinar la aptitud de un laboratorio para efectuar pruebas de diagnóstico específicas (punto 1.3. i)) se habla de prueba de idoneidad. Las pruebas de idoneidad son parte integrante de la mayoría de los programas de acreditación de laboratorios.
Los programas de pruebas de capacidad se basan en conjuntos definidos de materiales de prueba perfectamente caracterizados, a veces denominados grupos de muestras de control. Estos grupos de muestras se envían simultáneamente a los laboratorios participantes. Los resultados de las pruebas se reúnen y cotejan con los resultados esperados, a fin de determinar la aptitud de un laboratorio para realizar una prueba de diagnóstico y producir resultados correctos.
1.5. Acreditación de un laboratorio
Un programa de acreditación es un procedimiento oficial de reconocimiento de la calidad y aptitud de un laboratorio por una autoridad independiente. Para conservar ese reconocimiento, los laboratorios deben participar asiduamente en un programas de acreditación y obtener buenos resultados. La autoridad independiente concede o deniega el reconocimiento en función de requisitos preestablecidos de calidad y de aptitud.
En la fase inicial del procedimiento de acreditación se pide a los laboratorios que demuestren tener un nivel de calidad determinado y constante. Idealmente, para poder participar en un programa de evaluación de idoneidad, un laboratorio debe tener métodos de trabajo conformes a las prescripciones de ISO 9000 e ISO/IEC 17025 (normas generales de competencia para los laboratorios de diagnóstico o de calibración, 1990) o a las más específicas de la Norma de la OMSA. No obstante, se reconoce que para algunos laboratorios, por diversas razones, puede resultar difícil alcanzar un nivel tan elevado. La falta de acreditación oficial no debe impedir la participación en programas de evaluación de la idoneidad.
2. Organismo encargado de la acreditación y reconocimiento
Los programas de acreditación y de pruebas de idoneidad deben desarrollarse, siempre que sea posible, bajo la responsabilidad de una un organismo independiente, a fin de prevenir cualquier arbitrariedad en la concesión o en la denegación del reconocimiento.
La participación en un programa internacional de pruebas de idoneidad debe ser voluntaria. El hecho de no participar en ellas o de no obtener el reconocimiento no impedirá que un laboratorio efectúe pruebas de diagnóstico o que un país sea parte en acuerdos comerciales.
La participación y el reconocimiento serán concedidos por el organismo independiente a las partes en intercambios comerciales únicamente a petición del laboratorio o de la autoridad nacional participantes, o con su consentimiento.
El programa y el plan de pruebas pueden suponer gastos para los laboratorios participantes, a cambio de estos servicios.
3. Organización y gestión
El organismo coordinador debe documentar los detalles del plan de pruebas de idoneidad y su finalidad, los criterios para la admisión de los laboratorios interesados y el tratamiento de los resultados, de modo de garantizar la protección de los derechos de propiedad y la confidencialidad de la información.
Un director del programa de pruebas de idoneidad asumirá la responsabilidad general de la ejecución, la calidad y la seguridad de ese programa.
También incumbirá al director del programa velar por que los laboratorios involucrados en la producción de materiales de prueba cumplan los requisitos pertinentes formulados en los documentos ISO 9000 e ISO/IEC 17025.
Los empleados no deberán ser objeto de presiones o influencias que puedan influir en el análisis de los resultados de las pruebas de idoneidad o en el reconocimiento del laboratorio participante.
La supervisión y la seguridad necesarias estarán a cargo del personal involucrado en la producción y distribución de los materiales de prueba que se han de utilizar en el plan de pruebas de idoneidad, o bien en la recepción y el análisis de los resultados de las pruebas presentados por los laboratorios participantes.
4. Métodos de normalización
El método de prueba empleado para caracterizar los materiales de prueba usados en los grupos de muestras de control deberá alcanzar o rebasar las características mínimas de rendimiento diagnóstico requeridas para una prueba prescrita en el Manual de Pruebas de Diagnóstico y Vacunas para los Animales Terrestres de la OMSA.
El método de prueba deberá calibrarse en función de materiales de referencia internacionales, si éstos están disponibles. Asimismo, habrá que alentar a los laboratorios participantes a calibrar sus propias pruebas biológicas con arreglo a las mismas normas internacionales.
5. Selección y composición del juego de muestras de control
5.1. Principios generales
Para seleccionar los materiales que se han de incluir en el juego de muestras de control, la evaluación inicial de la condición y/o de la reactividad de las muestras será efectuada por el laboratorio productor, mediante el método normalizado.
Los materiales de prueba aceptados para ser incluidos en las pruebas de capacidad deberán ser sometidos a controles reiterados efectuados por varios analistas y a series de pruebas múltiples realizadas en distintos días. Habrá que determinar valores suficientes para garantizar la caracterización inequívoca del material usado en las pruebas y su homogeneidad.
5.2. Composición del juego de muestras
El número de muestras de control que constituyen un juego no está bien definido. Se determinará en función del tipo de análisis que se haya de aplicar a los resultados de las pruebas y de las cantidades requeridas para asegurar una validez estadística.
Sea cual sea el tipo de prueba que se realice, deberán incluirse como mínimo tres muestras:
i) una muestra fuertemente positiva inequívoca,
ii) una muestra escasamente positiva inequívoca y
iii) una muestra inequívocamente negativa.
Pero el uso de sólo tres muestras de este tipo daría resultados muy previsibles tras unas pocas series de pruebas de idoneidad. Por lo tanto, sería conveniente añadir al juego de muestras de control por lo menos otras dos muestras, que podrían variar entre dos series consecutivas de pruebas de idoneidad. Así se impediría que los laboratorios participantes pudieran anticipar los resultados esperados. Las muestras adicionales podrían ser distintas de las mencionadas o réplicas de éstas, o una combinación.
Cuando se esté planificando el proceso de preparación, puesta a prueba y distribución del material y los artículos, el proveedor facilitará, en su caso, los procedimientos y recursos necesarios para:
i) la selección del material;
ii) mantener un entorno apropiado para la preparación y puesta a prueba del material;
iii) la preparación del material;
iv) medición y puesta a prueba;
v) calibrado/validación del material y los métodos de medición;
vi) valorar la homogeneidad del material;
vii) valorar la estabilidad del material;
viii) organizar comparaciones entre laboratorios con los colaboradores, de ser necesario: (ver Nota 1 anterior);
ix) un almacenamiento en condiciones e instalaciones adecuadas;
x) envasado y etiquetado adecuados;
xi) transporte y distribución apropiados;
xii) análisis estadístico de los resultados de la prueba y asignación de valores de mensurandos e incertidumbres asociadas;
xiii) prestar un servicio de información a los participantes.
6. Análisis estadístico de las pruebas serológicas
6.1. Tipos de datos
La elección del análisis estadístico depende en parte del tipo de datos que suministra el método de prueba de que se trate. Los datos cualitativos, como “positivo”, “negativo” y/o “sospechoso”, son un tanto limitados desde el punto de vista de los procedimientos estadísticos aplicables. Los datos cuantitativos, tales como las titulaciones de punto final, y los datos semicuantitativos, como los porcentajes de inhibición, son más flexibles por lo que se refiere a los tipos de análisis estadístico posibles.
Cualquiera fuere el tipo de los datos que se hayan de analizar, es importante que los datos de todos los laboratorios participantes sean compatibles. En algunos casos se puede pedir que los laboratorios participantes utilicen una serie de diluciones específica o expresen su información en función de una misma norma de referencia.
6.2. Valores asignados
Pueden asignarse valores de dos maneras:
a) Asignación previa de un valor diana
En la selección inicial de materiales destinados al juego de muestras de control, el laboratorio productor habrá asignado a la muestra un valor, un ámbito de valores o una condición preliminares. Cuando se trata de datos cualitativos el valor asignado puede ser el único valor aceptable. Si tal es el caso, el laboratorio productor deberá verificar su condición mediante una serie de pruebas, a fin de confirmar con mayor certeza que el valor asignado es correcto. Sin embargo, el objetivo es que al menos el 80% de los laboratorios participantes en las pruebas de idoneidad obtengan el mismo resultado. En cuanto a los datos cuantitativos y semicuantitativos, el valor asignado se volverá a calcular a la luz de los resultados presentados por los laboratorios, y se adoptará el valor medio tras la eliminación de los valores aberrantes.
b) Asignación de un valor diana en base al valor consensuado de los resultados recibidos
6.3. Métodos estadísticos
En las comparaciones entre laboratorios se han aplicado muchos métodos estadísticos, algunos mucho más refinados que otros. Por regla general, las estadísticas que se apliquen deberán ser válidas, claras y significativas para los laboratorios participantes.
El análisis de frecuencia es un método sencillo e interesante para los laboratorios que desean comparar su desempeño con el de los demás participantes en el programa de pruebas de idoneidad.
Las mediciones de la varianza en un mismo laboratorio o entre laboratorios mediante índices de repetibilidad y reproducibilidad suelen suministrar información valiosa sobre la precisión y la fiabilidad de los métodos de prueba.
El análisis de Youden es un indicador útil de las fuentes de errores sistemáticos o aleatorios que pueden causar problemas en determinados laboratorios.
7. Criterios de suficiencia
Los criterios de decisión en cuanto a la suficiencia o insuficiencia de un laboratorio en una prueba de idoneidad deben estar claramente documentados. Deben tomar en consideración factores que pueden diferir en función de las enfermedades o de los tipos de pruebas. Una vez establecidos, los criterios se deben aplicar de manera uniforme.
Los tipos de análisis estadístico escogidos deben facilitar la toma de decisiones al término de las pruebas. Es preciso individualizar los laboratorios cuyos resultados rebasan los límites establecidos por medios estadísticos. Los resultados de las pruebas serológicas que podrían llevar a clasificar como falsamente negativo a un animal infectado deberán ser ponderados con los que pueden dar lugar a un dictamen falsamente positivo para un animal sano. En la mayoría de los casos, el primer tipo de error no deberá tolerarse, ya que indica que hay dificultades con la sensibilidad diagnóstica. En cambio, puede haber cierta tolerancia para conceder una calificación provisional a laboratorios que experimentan problemas con la especificidad diagnóstica.
8. Frecuencia de las pruebas de idoneidad
Se recomienda que las pruebas de idoneidad se efectúen dos veces por año. En función del país y de la enfermedad de que se trate, se deberán tomar en consideración los periodos de máxima actividad analítica. En la medida de lo posible, por lo menos una de las pruebas de capacidad deberá coincidir con periodos de gran actividad.
La reiteración de las pruebas de idoneidad a razón de dos por año brinda tiempo suficiente para que un laboratorio participante tome las disposiciones correctivas necesarias a fin de no perder su reconocimiento.
9. Reconocimiento de los laboratorios
Deben definirse claramente los criterios para conceder, denegar o retirar el reconocimiento de idoneidad.
10. Logística
10.1. Admisibilidad y aceptación
Los laboratorios deberán recibir una descripción de conjunto del plan de pruebas de idoneidad. Esta reseña deberá contener información detallada sobre la frecuencia de las pruebas, los compromisos y los plazos, los métodos de análisis de datos, el envío de los informes requeridos, los criterios de reconocimiento de la idoneidad, la forma de presentación de los resultados y la confidencialidad. Además, recibirán un formulario que deberán firmar y remitir al organismo coordinador, y en el que se indicará que el laboratorio acepta los requisitos y las condiciones del programa.
10.2. Notificación de las pruebas y envío de los juegos de muestras
Los laboratorios participantes deberán ser notificados de la siguiente prueba de idoneidad con por lo menos un mes de antelación. La notificación indicará la fecha prevista y el método de envío del juego de muestras de control. Los laboratorios de países que exigen autorizaciones para la importación de los juegos de muestras de control podrán requerir una mayor anticipación de la notificación.
Los materiales de las pruebas incluidos en las muestras de control deberán estar codificados a fin de no revelar el resultado esperado. La codificación puede ser alfabética o numérica. Cada laboratorio participante deberá recibir un juego de muestras que corresponde a una serie única de códigos, a fin de impedir la colusión entre laboratorios.
Todos los envíos deberán efectuarse por la vía más expedita y directa y cumplir la reglamentación de la IATA[3] relativa al transporte de material biológico.
Una vez efectuado el envío, se deberán comunicar a los laboratorios destinatarios los detalles pertinentes (esto es, el método de envío, el transportista, la factura de transporte aéreo, etc.) a fin de facilitar una rápida recuperación del material y los trámites administrativos a su llegada.
Se deberán reemplazar inmediatamente los juegos de muestras de control que lleguen deteriorados o en condiciones dudosas.
10.3. Realización de las pruebas y comunicación de los resultados
Se proporcionará a los laboratorios participantes un volumen adecuado de materiales de prueba y tiempo suficiente para que puedan analizar el juego de muestras de control de la manera que estimen conveniente. Las muestras podrán ser sometidas a pruebas más de una vez y por más de una persona del laboratorio participante. No obstante, sólo se deberá remitir al organismo coordinador un único juego de resultados. Normalmente, se designará a la persona responsable de la ejecución rutinaria de las pruebas para tratar el juego de muestras de control.
El juego de muestras de control irá acompañado por un juego completo de instrucciones relativas a la reconstitución, conservación y manipulación, con los requisitos especiales de las pruebas, la expresión de los datos y los plazos para la presentación de los resultados.
Los resultados se deberán enviar en el formato adecuado y en tiempo oportuno. El incumplimiento de estas condiciones podrá dar lugar a la eliminación del programa de pruebas de idoneidad y a la pérdida o al descenso del nivel del reconocimiento.
El organismo coordinador deberá acusar recibo de los resultados y notificar que los acepta para efectuar los análisis correspondientes.
10.4. Análisis de los resultados e informe
Una vez vencido el plazo fijado para la recepción de los resultados, su análisis y la presentación de los informes correspondientes deberán quedar finalizados a tiempo.
Se elaborará un informe general en el cual se reseñarán los resultados de todos los análisis, y que se distribuirá a todos los laboratorios participantes. Se asignará en forma aleatoria. un código a los laboratorios participantes para garantizar su anonimato en el informe general y se comunicará a cada laboratorio su código único para esa serie de pruebas de idoneidad.
Cada laboratorio recibirá asimismo una síntesis de sus propios resultados y el reconocimiento de su calificación. En este resumen se indicarán claramente todos los factores que contribuyan a cualquier modificación de su situación anterior. Si tal modificación es desfavorable, será especialmente importante señalar las causas reales o potenciales que hayan contribuido a adoptar esta medida. En ciertos casos puede ser pertinente enviar un segundo juego de muestras idéntico al primero, después de que se hayan tomado las medidas correctivas necesarias.
El reconocimiento de la aptitud del laboratorio también puede revestir la forma de un certificado oficial.
Todos los datos, resultados y análisis y el reconocimiento otorgado a los laboratorios participantes seguirán siendo confidenciales en todo momento.
11. Publicación
El objetivo fundamental de estas directrices consiste en eliminar barreras comerciales y no en crearlas. Es de prever que los laboratorios participantes que hayan obtenido un reconocimiento pleno de su idoneidad pedirán que el organismo independiente o el coordinador pongan a disposición de los interlocutores comerciales un comprobante oficial de su calificación. Esto se hará únicamente a petición del laboratorio participante o de las autoridades nacionales correspondientes, o con su consentimiento.
12. Referencias
ISO/IEC International Standard 17025 (2005). General requirements for the competence of testing and calibration laboratories. International Organisation for Standardisation (ISO)/International Electrotechnical Commission (ISO/IEC), ISO Central Secretariat, 1 rue de Varembé, Case Postale 56, CH – 1211, Geneva 20, Switzerland.
International Organisation for Standardisation (ISO) (1997). Proficiency testing by interlaboratory comparisons. Part 1: Development and operation of proficiency testing schemes. Part 2: Selection and use of proficiency testing schemes by laboratory accreditation bodies. ISO/International Electrotechnical Commission (ISO/IEC), Guide 43. ISO/IEC, Geneva, 19 pp.
ISO International Standards 9000:2005, 9001:2000; 9004:2000 (2000–2005). Quality management and quality assurance. International Organization for Standardization (ISO), ISO Central Secretariat, 1 rue de Varembé, Case Postale 56, CH – 1211, Geneva 20, Switzerland.
[1] ISO: International Organisation for Standardisation
[2] IEC: International Electrotechnical Commission
[3] IATA: Asociación Internacional de Transporte Aéreo
Criterios
Los criterios que se han de aplicar en la selección de instituciones para su designación como Centro de referencia de la OMSA son los siguientes:
- la aptitud, capacidad y buena disposición de la institución para prestar los servicios descritos en el Mandato de los Centros de referencia de la OMSA que constituyen la base de su relación con la Organización, incluyendo, por ejemplo, la capacidad de recibir muestras biológicas procedentes de otros Estados Miembros de la OMSA;
- la posición científica y técnica de la institución interesada a nivel nacional e internacional, la presencia de expertos veterinarios en los equipos científicos y, para los Laboratorios de Referencia, la conformidad con las normas de la OMSA y otras normas internacionales de aseguramiento de calidad de los laboratorios y de medidas de bioseguridad;
- el lugar que ocupa la institución dentro de las estructuras zoosanitarias, científicas o educativas del Estado Miembro;
- la calidad de su liderazgo científico y técnico, su reconocimiento internacional en el campo de su competencia, y, para los Centros colaboradores, el número de miembros del personal y sus calificaciones;
- la estabilidad prospectiva de la institución en términos de personal, actividades y financiamiento;
- la relación de trabajo que la institución ha desarrollado con otras instituciones a nivel nacional, regional y mundial;
- la pertinencia técnica y geográfica de la institución y sus actividades respecto a las prioridades del programa de la OMSA.
Reglamento interno
ARTÍCULO 1
Las candidaturas al título de Centro de referencia de la Organización mundial de sanidad animal (OMSA) podrán ser dirigidas al Director general por el Delegado del Miembro de la OMSA al que pertenece la institución interesada o por la Comisión Regional correspondiente.
ARTÍCULO 2
El director de la institución transmitirá al Director general una declaración de conflicto de interés de la institución y su personal que exponga los eventuales conflictos que pudiera tener en calidad de institución de la OMSA con una entidad comercial, según un procedimiento establecido por el Director general. El responsable del establecimiento debe comprometerse para que la institución y su personal respete la confidencialidad que se relaciona con la información a la cual tendrá acceso en el ejercicio de sus funciones y debe proporcionar al Director general un compromiso de confidencialidad.
Un laboratorio de referencia debe respetar los derechos de propiedad intelectual aplicables a las muestras recibidas y no debe utilizar los resultados, sin consentimiento, para ir más allá de las investigaciones epidemiológicas ni para decidir la estrategia de su control. En caso de resultado positivo para una de las enfermedades de la lista de la OMSA, el laboratorio de referencia dbe informar de inmediato al Delegado del Estado Miembro de la OMSA del cual proviene la muestra, así como la Sede de la OMSA.
ARTÍCULO 3
Tras el dictamen de la Comisión Regional y de la Comisión especializada pertinentes, el Director general presentará las candidaturas recibidas al Consejo para su aprobación. Las candidaturas serán seleccionadas en función de los criterios indicados en el anteriormente. Sin embargo, en principio, no se puede designar más de un laboratorio de referencia para el mismo agente patógeno o para la misma enfermedad en un mismo país. De igual forma, no se puede designar más de un Centro colaborador para el mismo dominio o la misma especialidad en una misma región, o excepcionalmente, en una misma subregión.
ARTÍCULO 4
Las candidaturas seleccionadas serán presentadas por el Consejo a la Asamblea para su aprobación.
ARTÍCULO 5
El Director general notificará a las instituciones aprobadas su designación como Centro de referencia de la OMSA con el título formal que será utilizado en tanto que Centro de referencia de la OMSA. El Director general informará también en consecuencia al Delegado permanente del respectivo País Miembro.
ARTÍCULO 6
Esta notificación otorgará a la institución el derecho de utilizar el título de “Laboratorio de Referencia de la OMSA” o “Centro Colaborador de la OMSA” , así como el emblema de la OMSA en todos los documentos que el laboratorio elabore en su calidad oficial. De igual forma en el caso de los Laboratorios de referencia, se le otorgará el derecho al título de Experto de la OMSA al especialista designado.
ARTÍCULO 7
El Director el Centro de referencia es enteramente responsable de la implementación del mandato y, en el caso de los Centros colaboradores, este debe ser la única interfaz con la OMSA. En un Laboratorio de referencia, el experto es responsable de la implementación de los aspectos técnicos del mandato y pude delegar ciertas responsabilidad específicas a otros expertos según una base ad hoc. Los expertos asociados a los Centros de referencia ejercen su cargo conforme al reglamento aplicable a los Expertos de la OMSA.
ARTÍCULO 8
Los Centros de referencia de la OMSA deben comprometerse a suministrar un informe de actividad sucinto al Director general al término de cada año civil de su mandato, según un modelo proporcionado por la Sede de la OMSA. Dicho informe será entregado a todos los Estados Miembros.
ARTÍCULO 9
Un Centro de referencia puede ser revocado en cualquier momento. Su designación debe ser retirada si el Centro de referencia no se encuentra en conformidad con las disposiciones del mandato definidas en el presente Reglamento. En este caso, el Director general de la OMSA, luego de consultar con la Comisión especializada apropiada, propone la revocación a la Asamblea.
ARTÍCULO 10
Cualquier modificación importante que se produzca en la institución y que pueda reducir la competencia del Centro de referencia (especialmente el cambio de personal o de recursos humanos o financieros), deberá ser inmediatamente señalada al Director general, quien consultará con la Comisión Regional y la Comisión especializada pertinentes si la institución conservará el título de Centro de referencia.
Los laboratorios de referencia de la OMSA deben demostrar su liderazgo científico y su capacidad de cumplir su mandato. Todos los candidatos deben ser, preferiblemente, laboratorios nacionales de referencia; deben ser capaces de recibir muestras de otros países para efectuar pruebas de diagnóstico; deben demostrar su capacidad e intención de organizar pruebas de aptitud y no simplemente participar en ellas; deben ser capaces de proporcionar servicios de diagnóstico de confirmación, materiales de referencia, capacitación, etc., a escala internacional; además, el experto designado debe haber publicado varios artículos recientes en revistas profesionales que cuenten con un comité de revisión. Un laboratorio de referencia activo exige la participación de expertos que trabajan en diferentes áreas en torno a una misma enfermedad o patógeno. Se entiende que el experto designado es un integrante destacado de tal equipo multidisciplinario que puede consultar a los demás miembros del equipo con competencias diversas en respuesta a solicitudes recibidas y es, al mismo tiempo, el único punto de contacto para toda correspondencia con los Miembros de la OMSA y otros interlocutores. El artículo 7 del reglamento interno de los centros de referencia consigna esta idea al indicar que, “en un laboratorio de referencia, el experto es responsable de la implementación de los aspectos técnicos del mandato y pude delegar ciertas responsabilidades específicas a otros expertos según una base ad hoc”.
Se presentarán las candidaturas 45 días antes de la fecha prevista para la reunión de la comisión pertinente (ambas la Comisión de Normas Biológicas como la Comisión de Normas Sanitarias para los Animales Acuáticos se reúnen en febrero y septiembre; los plazos son por lo tanto mediados de diciembre y mediados de julio. Este plazo de 45 días deja tiempo suficiente a la OMSA para filtrar, traducir al inglés si procede y tramitar los expedientes para que la comisión los examine. Se deben respetar las fechas límite escrupulosamente, a fin de que los miembros de la comisión los puedan estudiar detenidamente antes de la reunión. Los expedientes que lleguen una vez transcurrido el plazo serán examinados en la siguiente reunión.
Las solicitudes deberán presentarse de conformidad con el Artículo 1 del reglamento interno y mencionarán la siguiente información:
Administración y gestión
1. Nombre del experto (currículum vítae empleando este modelo).
2. Nombre y dirección del laboratorio (número de teléfono y dirección de correo electrónico [sitio web, en su caso]).
3. Nombre del Jefe de laboratorio (agente responsable).
4. Demostrar que existen disposiciones normativas y presupuestarias, adoptadas para garantizar la sostenibilidad y el funcionamiento del laboratorio.
5. Documentos que dejen constancia (certificados) de acreditación conforme a la norma ISO 17025 o un sistema equivalente de gestión de calidad en los laboratorios de diagnóstico, idealmente con pruebas pertinentes incluidas en el ámbito de la acreditación.
Saber hacer y experiencia técnica
6. Bridar un panorama de la pericia disponible para la enfermedad o patógeno dentro del equipo multidisciplinario en el que trabaja el experto; disciplinas, número de expertos en cada una de ellas, nivel de experiencia.
7. Detallar la experiencia en el campo de las pruebas de diagnóstico de la enfermedad de acuerdo con las normas de la OMSA a escala nacional e internacional (indicar el número aproximado de pruebas realizadas anualmente para cada técnica).
8. Aportar información adicional sobre la pericia en técnicas de diagnóstico (técnicas de caracterización del agente, técnicas moleculares, técnicas de anticuerpos monoclonales, etc.), epidemiología y control de la enfermedad.
9. Detallar la experiencia en la estandarización y validación de las pruebas de diagnóstico.
10. Demostrar la capacidad de producción de reactivos (proporcionar detalles acerca de las reservas actuales de reactivos para la enfermedad).
11. Demostrar la capacidad de envío y recepción internacional oportuna de muestras, de acuerdo con los requisitos para el envío postal y el embalaje de materiales biológicos descritos en el Manual de las Pruebas de Diagnóstico y de las Vacunas para los Animales Terrestres de la OMSA, así como en el Código Sanitario para los Animales Terrestres o el Código Sanitario para los Animales Acuáticos de la OMSA.
12. Lista de los proyectos de investigación y de elaboración de métodos sobre la enfermedad finalizados.
13. Lista de las pruebas de aptitud interlaboratorios que el laboratorio organiza, y en las que participa, con regularidad.
14. Detallar la experiencia en los campos de formación y consulta sobre la enfermedad en los dos últimos años (cursillos impartidos, número de personas formadas, ejemplos de consultas internacionales).
15. Lista de las reuniones científicas que el laboratorio ha organizado y en las que ha participado.
16. Lista de contribuciones a documentos de referencia (capítulos para el Manual de las Pruebas de Diagnóstico y de las Vacunas para los Animales Terrestres, el Manual de Pruebas de Diagnóstico para los Animales Acuáticos de la OMSA, fichas de enfermedades, etc.).
Colaboración, confidencialidad, conflictos
17. Lista de acuerdos de colaboración con otros laboratorios, centros u organizaciones.
18. Garantizar que el personal respeta la confidencialidad de ciertos temas, resultados o comunicaciones y también que se toman medidas respecto a los conflictos potenciales de interés, por medio de las declaraciones que se soliciten.
19. Remitir el compromiso de confidencialidad y la declaración de conflicto de intereses firmadas por el director de la institución en nombre de la institución, de conformidad con el reglamento para los laboratorios de referencia de la OMSA, disponible en el Marco de Referencia – OMSA – Organización Mundial de Sanidad Animal.
La candidatura será tramitada por la OMSA de conformidad con los Artículos 2, 3 y 4 del Reglamento Interno.
Deberá incluirse un breve resumen de las actividades pertinentes para la condición de Laboratorio de Referencia de la OMSA (una página como máximo).
Los expedientes se limitarán a un máximo de 20 páginas de formato A4, a espacio simple y en Times New Roman de 10pt. Se habrá redactado en uno de los idiomas oficiales de la OMSA (inglés, francés o español).
* Plazo en función de las fechas previstas para las reuniones de la comisión pertinente
Información relacionada con el procesamiento de datos personales
La OMSA, en su calidad de responsable del tratamiento de datos, procesará sus datos de contacto e identificación obtenidos de fuentes privadas para la ejecución de su mandato, incluyendo a efectos de comunicaciones, gestión de reuniones y formación. Además, al publicar las listas de los centros de referencia designados por la OMSA y los informes anuales de sus actividades, la OMSA incluirá sus datos personales en el sitio web de la OMSA. Los datos recabados serán tratados internamente para los fines antes mencionados. Además, como organización internacional, transferimos datos personales dentro de nuestras diversas oficinas, así como a proveedores de servicios y socios externos para realizar tareas en nuestro nombre y ayudarnos a cumplir con nuestro mandato. Sus datos personales se conservarán hasta que dejen de ser relevantes. Tiene derecho a acceder y rectificar sus datos personales, así como a solicitar su supresión, oponerse al tratamiento y obtener la portabilidad de los datos en determinadas circunstancias. Puede encontrar más información sobre el procesamiento y sus derechos en nuestra Política de privacidad.
En el contexto del desempeño de sus obligaciones como experto de la OMSA, es posible que ocasionalmente se le solicite que procese datos personales en nombre de la OMSA.
Si se le solicita que procese datos personales en nombre de la OMSA, deberá proporcionar garantías suficientes en cuanto a la implementación de las medidas técnicas y organizativas adecuadas, de modo que las operaciones de procesamiento cumplan con las normas generalmente aceptadas en materia de protección de datos.
Al procesar datos personales en nombre de la OMSA, declara que brinda suficientes garantías en cuanto a la implementación de las medidas técnicas y organizativas adecuadas, para que las operaciones de procesamiento cumplan íntegramente con los requisitos de la normativa aplicable en materia de protección de datos personales.
Se acuerda expresamente que usted:
- procesará los datos únicamente para los fines cubiertos por su mandato y las instrucciones relativas al tratamiento enviadas por la OMSA;
- procesará los datos personales siguiendo instrucciones documentadas de la OMSA, incluso con respecto a la ubicación del alojamiento y las transferencias a terceros países;
- garantizará la confidencialidad de los datos personales tratados bajo instrucción de la OMSA;
- ayudará a la OMSA, mediante las medidas técnicas y organizativas adecuadas y, en la medida de lo posible, a cumplir con su obligación de responder a las solicitudes de las personas relevantes en relación con sus derechos (derechos de acceso, rectificación, supresión y oposición, restricción del tratamiento, portabilidad de los datos). y notificar las violaciones de datos personales cuando lo considere oportuno;
- tomará e implementará todas las medidas apropiadas para garantizar un nivel de seguridad adaptado al riesgo presentado por las operaciones de procesamiento;
- eliminará, a solicitud de la OMSA, todos los datos personales o los restituirá a la OMSA o al nuevo experto una vez finalizado su mandato; la restitución de dichos datos deberá ir acompañada de la destrucción por su parte de todas las copias existentes en su sistema de información.
Orientación para la gestión de las redes de los Laboratorios de Referencia de la OMSA
Introducción
La red mundial de Centros de Referencia de la OMSA constituye el núcleo de la excelencia científica de la OMSA. La Primera Conferencia Mundial de Laboratorios de Referencia y Centros Colaboradores de la OMSA (celebrada en Florianopolis, Brasil, en 2006) recomendó que se desarrollara una red de Laboratorios de Referencia y Centros Colaboradores de la OMSA con el objetivo de armonizar e intercambiar datos, información y material de referencia para mejorar la vigilancia y el control de enfermedades en el mundo entero.
La Segunda Conferencia Mundial de Laboratorios de Referencia y Centros Colaboradores de la OMSA (celebrada en París, en 2010) alentó a las redes de Laboratorios de Referencia y Centros Colaboradores a seguir trabajando juntas a fin de reforzar la cooperación multilateral, en particular, con la finalidad de producir e incrementar la disponibilidad de material biológico de referencia validado. Para reforzar dicha colaboración, los Laboratorios de Referencia y Centros Colaboradores debían seguir compartiendo conocimientos, material de referencia y pericia en beneficio de los Países Miembros de la OMSA.
El mandato aprobado en mayo de 2011 exigía explícitamente que los Laboratorios de Referencia de la OMSA estableciesen y mantuviesen una red con otros Laboratorios de Referencia designados para el mismo patógeno. Para más información sobre los mandatos de los Laboratorios de Referencia de la OMSA, consulte el siguiente enlace.
La OMSA ha detectado que se necesita más orientación sobre la coordinación de las redes de los Laboratorios de Referencia de la OMSA. El objetivo consiste en garantizar opiniones de expertos unificadas y asesorar a los Países Miembros de la OMSA mediante un intercambio de información mejorado.
La red de Laboratorios de Referencia de la OMSA deberá asegurar que todos los laboratorios obtengan resultados congruentes mediante el cumplimiento de las normas de la OMSA, el intercambio de material de referencia en el seno de la red y la participación en las debidas pruebas de competencia. El trabajo en red también ofrece oportunidades de intercambios de conocimientos y experiencia, respaldo recíproco y desarrollo de colaboraciones científicas. Igualmente, mejorará la credibilidad y multiplicará la visibilidad de los Laboratorios de Referencia de la OMSA en el mundo, y atraerá la participación de otros laboratorios de referencia de los Países Miembros de la OMSA.
Según el caso, la sede de la OMSA podrá invitar a los Laboratorios de Referencia existentes a reunirse, física o telefónicamente, con el fin de contribuir a crear una red, designar una secretaría y seguir las presentes orientaciones.
Recomendaciones
- El trabajo en red entre los Laboratorios de Referencia de la OMSA forma parte de su mandato. Cuando se haya designado a dos o más Laboratorios de Referencia de la OMSA para el mismo patógeno, deberá establecerse una red. La participación en dicha red será obligatoria para los Laboratorios de Referencia de la OMSA. Aunque solo los Laboratorios de Referencia de la OMSA deberán rendir cuentas ante la Organización, otros laboratorios de referencia podrán participar, en su caso, en algunas de las actividades de la red.
- La red deberá contar con una secretaría (que se notificará oficialmente a la OMSA), con sede en uno de los Laboratorios de Referencia partícipes, que servirá de enlace con la sede de la OMSA. Además, la secretaría será responsable de la coordinación, dirección y rendición de cuentas de la red. La secretaría podrá alternarse entre los diversos laboratorios participantes (p. ej., cada tres años). Es responsabilidad de la secretaría de la red gestionar los conflictos de intereses y las cláusulas de confidencialidad si la red lo considera necesario sin la intervención de la OMSA.
- La secretaría de cada red deberá contar con un plan de trabajo bien definido y presentará al Director General de la OMSA un informe anual de sus actividades: logros, obstáculos, iniciativas futuras (los laboratorios individuales podrán hacer referencia al informe de la red en su informe anual en calidad de Laboratorios de Referencia de la OMSA).
- Cuando la red organice reuniones, deberá permitirse la participación como observadores de personal de la OMSA, y la secretaría redactará un informe de la reunión que deberá comunicarse a la sede de la OMSA.
- Si surgiera una discrepancia o un desacuerdo que no pudiese resolverse en el seno de la red, la secretaría deberá informar sin dilación a la sede de la OMSA, que informará en consecuencia a la Comisión de Normas Biológicas.
- Condiciones para la inclusión de enlaces a portales de redes en el sitio web de la OMSA:
- La red podrá crear un portal para difundir información sobre sus actividades. En ese caso, deberá pedir formalmente al Director General de la OMSA que se añada al sitio web de la Organización un enlace a su portal.
- El portal de la red deberá respetar las pautas de presentación gráfica y otras normas aplicables de la OMSA.
- Cualquier cambio sustancial del portal de la red deberá notificarse previamente a la OMSA.
- La sede de la OMSA se reserva el derecho de recomendar cambios en el contenido del portal de la red si lo estima conveniente y de retirar en todo momento el enlace al portal de la red, presentando las razones que la motivan a la secretaría de la red.
- Los informes y actividades de la red reflejan los puntos de vista de los integrantes de la red y no necesariamente los de la OMSA.
Punto de contacto de la OMSA para las redes:
Sara Linnane
Departamento Científico
Organización Mundial de Sanidad Animal (OMSA)
12, rue de Prony
75017 Paris, Francia
E-mail: [email protected]